En chimie, les forces de van der Waals sont une sorte de force intermoléculaire. Une force intermoléculaire est une force relativement faible qui maintient les molécules ensemble. Les forces de Van der Waals sont le type de force intermoléculaire le plus faible. Elles portent le nom du scientifique néerlandais Johannes Diderik van der Waals (1837-1923).
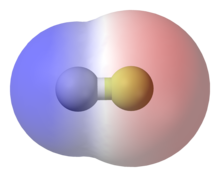
Les électrons chargés négativement sont en orbite autour des molécules ou des ions. Les électrons créent des charges légèrement différentes d'une extrémité de la molécule à l'autre. Ces légères différences sont appelées charges partielles, comme δ- ou δ+.
Le terme est parfois utilisé de manière vague comme synonyme de toutes les forces intermoléculaires. Les forces de Van der Waals sont relativement faibles par rapport aux liaisons covalentes, mais jouent un rôle fondamental dans la chimie supramoléculaire, les enzymes, la science des polymères, la nanotechnologie, la science des surfaces et la physique de la matière condensée. Les forces de Van der Waals définissent de nombreuses propriétés des composés organiques, notamment leur solubilité.

