Une batterie convertit l'énergie chimique en énergie électrique par une réaction électrochimique entre deux électrodes (l'anode et la cathode) séparées par un électrolyte. Les produits chimiques sont généralement contenus à l'intérieur de la batterie et produisent une tension continue : le courant circule dans un seul sens et ne change pas de direction, contrairement au courant alternatif fourni par le réseau domestique.
Fonctionnement
À l'intérieur d'une batterie, une réaction chimique libère des électrons à l'anode et en capte à la cathode. Cette séparation de charges crée une différence de potentiel (tension) entre les bornes. Lorsque la batterie est reliée à un circuit, les électrons circulent du pôle négatif vers le pôle positif via le circuit externe, fournissant de l'énergie aux appareils connectés. L'électrolyte permet le transport des ions à l'intérieur de la batterie pour maintenir l'équilibre des charges.
Types de batteries
On distingue principalement deux grandes familles :
- Batteries primaires (non rechargeables) : elles sont jetées lorsqu'elles sont déchargées. Exemples courants : piles alcalines (AA, AAA), piles zinc-carbone, et certaines piles au lithium non rechargeables. Elles sont pratiques pour des usages occasionnels ou de faible consommation.
- Batteries secondaires (rechargeables) : elles peuvent être rechargées et réutilisées plusieurs fois. Exemples : plomb-acide (batteries de démarrage, onduleurs), NiMH (appareils portables, piles rechargeables AA), lithium-ion et lithium-polymère (téléphones, ordinateurs portables, véhicules électriques). Ces technologies diffèrent par leur densité d'énergie, leur durée de vie et leurs contraintes de sécurité.
Caractéristiques techniques importantes
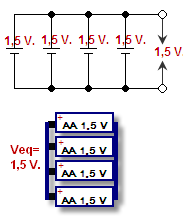
- Tension nominale : valeur typique fournie par une cellule (par ex. ≈1,5 V pour une pile alcaline, ≈3,6–3,7 V pour une cellule Li-ion).
- Capacité : exprimée en ampères-heures (Ah) ou milliampères-heures (mAh), elle indique la quantité d'électricité stockée.
- Énergie : exprimée en wattheures (Wh) = tension × capacité, mesure l'énergie totale disponible.
- Courant de décharge : courant maximum que la batterie peut fournir sans dommage ; lié à la résistance interne.
- Durée de vie en cycles : nombre de cycles charge/décharge utiles avant que la capacité ne chute significativement (quelques centaines à plusieurs milliers selon la chimie).
- Autodécharge : perte d'énergie au repos ; varie selon la chimie (plus faible pour le lithium, plus élevée pour NiMH).
Applications
- Appareils portables : téléphones, ordinateurs portables, tablettes (principalement Li-ion/LiPo).
- Transports : voitures électriques (grandes batteries Li-ion), vélos électriques, scooters.
- Stockage d'énergie stationnaire : systèmes de stockage pour panneaux solaires, onduleurs domestiques.
- Équipements d'appoint et de secours : onduleurs (UPS), batteries plomb-acide ou lithium adaptées.
- Équipements portatifs et consommables : télécommandes, jouets, lampes de poche (piles primaires).
Conseils d'utilisation et sécurité
- Respecter les recommandations du fabricant pour le chargeur et la température de charge. Ne pas utiliser un chargeur inadapté.
- Éviter les décharges profondes fréquentes pour certaines chimies (par ex. plomb-acide) ; pour le Li-ion, éviter de laisser la batterie totalement déchargée longtemps.
- Stocker à l'abri de la chaleur et préférer un état de charge partiel (environ 40–60 %) pour un stockage long terme des batteries lithium.
- Ne pas court-circuiter, percer, écraser ou exposer à une flamme : risque d'incendie ou d'explosion, surtout avec les batteries lithium.
- En cas de surchauffe, gonflement, fuite ou odeur anormale, cesser l'utilisation et manipuler avec précaution.
Recyclage et impact environnemental
Les batteries contiennent des métaux et des produits chimiques potentiellement dangereux (plomb, cadmium, lithium, électrolytes organiques). Il est important de les recycler via les filières appropriées : points de collecte en magasin, déchetteries ou programmes municipaux. Le recyclage permet de récupérer des métaux précieux, de réduire l'extraction de ressources et de limiter la pollution.
Remarques pratiques
- Le mot « pile » est souvent employé dans le langage courant pour désigner une batterie. Techniquement, une pile peut désigner une seule cellule tandis que « batterie » désigne un ensemble de cellules, mais l'usage courant mélange ces termes.
- Le choix d'une batterie dépend de l'application : priorité à la densité d'énergie (pour l'autonomie), à la densité de puissance (pour les accélérations), à la durée de vie cyclique, au coût et à la sécurité.
En résumé, une batterie transforme l'énergie chimique en électricité continue et existe en plusieurs chimies adaptées à des usages variés. Bien utilisée et recyclée correctement, elle est un élément clé des appareils modernes et de la transition énergétique.