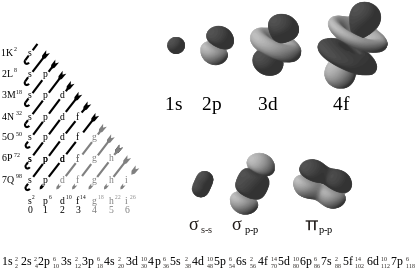
Les orbitales atomiques sont les endroits entourant le noyau d'un atome où les électrons sont le plus susceptibles de se trouver à un moment donné. Il s'agit d'une fonction mathématique qui décrit le comportement ondulatoire d'un ou de deux électrons dans un atome.
Le mot "orbital" est utilisé car on pensait que les électrons se comportaient de la même manière que le système solaire, où le noyau est comme le soleil et les électrons orbitent comme les planètes.
Le nombre d'orbitales atomiques d'un élément est défini par la période dans laquelle se trouve l'élément. Les électrons se déplacent entre les orbitales en fonction de la vitesse à laquelle ils se déplacent et du nombre d'autres électrons.
En théorie atomique et en mécanique quantique, une orbite atomique est un nombre quantique. Chacune de ces orbitales peut être occupée par un ou deux électrons. La façon dont les orbitales sont disposées est liée à la configuration des électrons des atomes. Elles ont été dérivées des descriptions fournies par les premiers spectroscopistes de certaines raies spectroscopiques de métaux alcalins comme étant nettes, principales, diffuses et fondamentales.