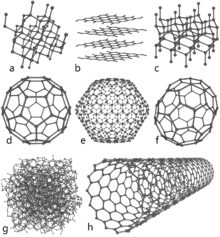
Il existe plusieurs allotropes de carbone. Le diamant et le graphite sont les plus connus. Le graphite est un conducteur, un semi-métal (un élément qui est en partie un métal et en partie un non métal, comme le phosphore noir et le sélénium gris). Il peut être utilisé, par exemple, comme matériau dans les électrodes d'une lampe à arc électrique. Le graphite est la forme la plus stable de carbone solide jamais découverte.
Les allotropes sont différentes formes d'un même élément chimique. Tous les éléments sont constitués uniquement de leurs propres atomes. Toute différence physique est due à la façon dont les atomes sont reliés entre eux. De nombreux éléments présentent une allotropie parce que les atomes peuvent être reliés entre eux de plusieurs façons. Il existe également différentes façons d'agencer les molécules pour former des structures plus grandes.
Le diamant est l'un des allotropes de carbone les plus connus. Sa dureté et sa grande dispersion de la lumière en font un bon matériau pour la bijouterie. Il a également des utilisations industrielles. Le diamant est le minéral naturel le plus dur connu. Cela en fait un excellent abrasif. Le diamant conserve également bien son éclat. Le diamant et le graphite ont tous deux un point de fusion extrêmement élevé, ce qui est inhabituel pour un élément non métallique.