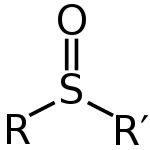
Un sulfoxyde est une molécule qui possède un atome de soufre lié à deux carbones et un atome d'oxygène. Il provient de l'oxydation des thioéthers, sans aller jusqu'à la sulfone. Comme de nombreuses molécules contenant du soufre, le sulfoxyde peut parfois avoir une odeur très forte.
Les sulfoxydes peuvent être écrits avec la formule générale R-S(=O)-R'. Le soufre a une double liaison avec l'oxygène, et des liaisons simples avec les carbones. Il ne reste donc qu'une seule paire sur l'atome. Cela signifie que la forme de cet atome est tétraédrique. Cela signifie également que le soufre peut être un centre chiral. Les sulfoxydes sont utilisés comme de bons ligands pour les métaux de transition.
Une molécule importante de ce type est le sulfoxyde de diméthyle. Elle est également appelée DMSO. Il est utilisé comme solvant pour de nombreuses réactions, notamment en biochimie.