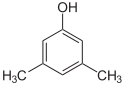
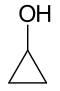
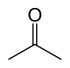
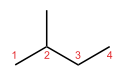Les isomères fonctionnels sont l'un des isomères structurels. Deux composés en isomérie fonctionnelle ont la même formule moléculaire (le nombre de chaque atome est le même, comme le cyclohexane:C
6H
12 et 1-hexène:C
6H
12). Mais les atomes sont reliés d'une autre manière, de sorte que les groupements sont différents. Nous appelons ces groupes d'atomes des groupes fonctionnels, des fonctionnalités ou des fractions. On peut aussi dire que deux composés qui ont la même formule moléculaire, mais qui ont des groupes fonctionnels différents, sont des isomères fonctionnels.
Par exemple, la formule chimique du cyclohexane et du 1-hexène est C6H12. Nous les appelons des isomères de groupes fonctionnels parce que le cyclohexane est un cycloalcane et l'hex-1-ène est un alcène.
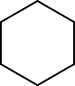
| Exemple d'isomérie de groupe fonctionnel |
| 
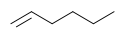
| 
|
| Cyclohexane | 1-hexène |
Pour que deux molécules soient des isomères fonctionnels, elles doivent contenir des groupes clés d'atomes disposés de manière particulière. Certains des meilleurs exemples proviennent de la chimie organique. C2H6O est une formule moléculaire. Selon la façon dont les atomes sont disposés, il peut représenter deux composés différents : l'éther diméthylique CH3-O-CH3 ou l'éthanol CH3CH2-O-H. L'éther diméthylique et l'éthanol sont des isomères fonctionnels. Le premier est un éther. La fonctionnalité chaîne carbone-oxygène-chaîne carbonée est appelée un éther. Le second est un alcool. La fonctionnalité chaîne carbone-oxygène-hydrogène est appelée un alcool.
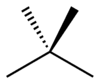
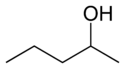
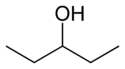
Si les fonctionnalités restent les mêmes, mais que leurs emplacements changent, les isomères structurels ne sont pas des isomères fonctionnels. Le 1-propanol et le 2-propanol sont des isomères structurels, mais ils ne sont pas des isomères fonctionnels. Tous deux sont des alcools. Le groupe fonctionnel (chaîne de carbone O-H) est présent dans ces deux composés, mais ils ne sont pas identiques.
Si certains chimistes utilisent indifféremment les termes d'isomère structurel et d'isomère fonctionnel, tous les isomères structurels ne sont pas des isomères fonctionnels.
Les isomères fonctionnels sont le plus souvent identifiés en chimie à l'aide de la spectroscopie infrarouge. Le rayonnement infrarouge correspond aux énergies associées principalement à la vibration moléculaire. La fonctionnalité de l'alcool a une vibration très distincte appelée OH-stretch qui est due à la liaison hydrogène. Tous les alcools sous forme liquide et solide absorbent le rayonnement infrarouge à certaines longueurs d'onde.
Les composés ayant les mêmes groupes fonctionnels absorbent tous certaines longueurs d'onde de la lumière infrarouge en raison des vibrations associées à ces groupes. En fait, le spectre infrarouge est divisé en deux régions. La première partie est appelée la région des groupes fonctionnels. L'éther diméthylique et l'éthanol auraient des spectres infrarouges différents dans la région du groupe fonctionnel.
La deuxième partie du spectre infrarouge est appelée la région des empreintes digitales ; elle est associée aux types de mouvement permis par la symétrie de la molécule et influencés par les énergies de liaison. La région de l'empreinte digitale est plus spécifique à un composé individuel. Même si le 1-propanol et le 2-propanol ont des spectres infrarouges similaires dans la région du groupe fonctionnel, ils diffèrent dans la région de l'empreinte digitale.
En termes simples, les isomères fonctionnels sont des isomères structurels qui ont différents groupes fonctionnels comme l'alcool et l'éther.