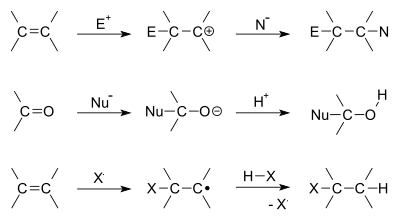
En chimie organique, une réaction d'addition se produit lorsque deux molécules se rejoignent pour en faire une plus grosse. Cela ne peut se produire que lorsque l'une des molécules a déjà une double ou une triple liaison. Il peut s'agir de liaisons carbone-carbone ou même carbone-oxygène, carbone-azote et autres. L'une des deux molécules est appelée nucléophile, et c'est elle qui donne les électrons à l'autre pour créer la nouvelle liaison. L'autre molécule est appelée électrophile, et c'est celle qui reçoit les électrons.
Une réaction d'addition est l'opposé d'une réaction d'élimination. Des exemples courants de réactions d'addition sont l'addition d'eau par une double liaison et l'attaque nucléophile d'un carbonyle.