Une réaction sigmatropique en chimie organique est une réaction péricyclique. Une réaction sigmatropique n'utilise pas de catalyseur et implique une seule molécule (un processus intramoléculaire non catalysé). Elle transforme une liaison σ en une autre liaison σ. Le nom sigmatropique est le résultat d'une combinaison du nom "sigma", établi de longue date pour les liaisons simples carbone-carbone, et du mot grec tropos, qui signifie tour. Il s'agit d'une réaction de réarrangement qui signifie que les liaisons d'une molécule se déplacent entre les atomes sans qu'aucun atome ne quitte la molécule ou que de nouveaux atomes n'y soient ajoutés. Dans une réaction sigmatropique, un substituant passe d'une partie d'un système lié à π à une autre partie dans une réaction intramoléculaire avec réarrangement simultané du système π. Les véritables réactions sigmatropiques ne nécessitent généralement pas de catalyseur. Certaines réactions sigmatropes sont catalysées par un acide de Lewis. Les réactions sigmatropes ont souvent des catalyseurs à base de métaux de transition qui forment des intermédiaires dans des réactions analogues. Les réarrangements sigmatropiques les plus connus sont le réarrangement de Cope [3,3], le réarrangement de Claisen, le réarrangement de Carroll et la synthèse d'indole de Fischer.
Transposition sigmatropique
Vue d'ensemble des décalages sigmatropiques
Nomenclature des changements sigmatropiques Woodward-Hoffman
Une notation spéciale est utilisée pour décrire les changements sigmatropiques. Un numéro de position est attribué à chacun des atomes de carbone du squelette de la molécule. Les réarrangements sigmatropiques sont décrits par un terme d'ordre [i,j]. Cela signifie la migration d'une liaison σ adjacente à un ou plusieurs systèmes π vers une nouvelle position (i-1) et (j-1) des atomes enlevés de l'emplacement original de la liaison σ. Lorsque la somme de i et j est un nombre pair, cela indique l'implication d'une chaîne d'atomes C neutre. Un nombre impair suggère qu'il y a un atome C chargé ou une paire d'hétéroatomes isolés remplaçant une double liaison carbone-carbone. Ainsi, les décalages [1,5] et [3,3] deviennent des décalages [1,4] et [2,3] avec des hétéroatomes, tout en préservant les considérations de symétrie. Les hydrogènes sont omis dans le troisième exemple par souci de clarté.

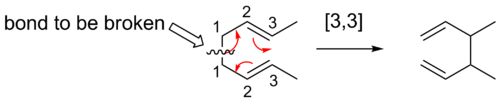
Voici un moyen de trouver l'ordre d'un réarrangement sigmatropique donné. La première étape consiste à donner des nombres à chaque atome en commençant par les atomes de la liaison rompue comme atome 1. Les chimistes comptent les atomes dans chaque direction depuis la liaison rompue jusqu'aux atomes qui forment la nouvelle liaison σ dans le produit. Les nombres qui correspondent aux atomes formant la nouvelle liaison sont ensuite séparés par une virgule et placés entre parenthèses. Cela crée le descripteur d'ordre de réaction sigmatropique.
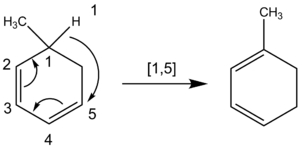
Les chimistes comptent également les atomes lorsqu'ils désignent un déplacement sigmatropique où un atome d'hydrogène se déplace. La chaîne de carbone ne se brise pas lors de la migration d'un atome d'hydrogène. Ainsi, les chimistes comptent tous les atomes impliqués dans la réaction plutôt que seulement les atomes les plus proches. Par exemple, la migration suivante des atomes d'hydrogène est d'ordre [1,5], obtenue en comptant dans le sens inverse des aiguilles d'une montre dans le système π, plutôt que l'ordre [1,3] dans le groupe CH2 du cycle qui serait obtenu par erreur si on comptait dans le sens des aiguilles d'une montre.
Changements supra-faciaux et antarafaciaux
Les chimistes ont étudié les réactions sigmatropes où le groupe migrant possède un stéréocentre. En principe, tous les déplacements sigmatropiques peuvent se produire avec la même géométrie (rétention) ou la géométrie opposée (inversion) du groupe migrant. Cela dépend si le lobe de liaison original de l'atome migrateur ou son autre lobe est utilisé pour former la nouvelle liaison.
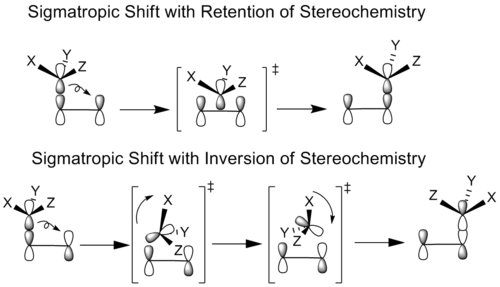
En cas de rétention stéréochimique, le groupe migrant se traduit sans rotation par la position de liaison. Dans le cas d'une inversion stéréochimique, le groupe migrant tourne et se déplace pour atteindre sa conformation de liaison.
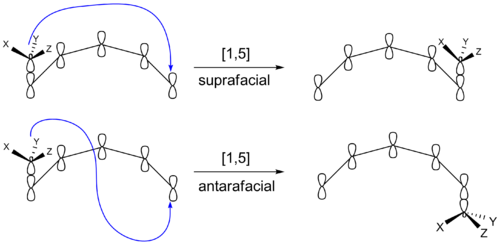
Une réaction sigmatropique peut aussi produire des produits ayant une stéréochimie différente. Le groupe migrant peut rester sur la face originale du système π après s'être recollé. Il peut aussi aller sur la face opposée du système π. Si le groupe migrateur reste sur la même face du système π, le déplacement est connu sous le nom de suprafacial. Si le groupe migrant se déplace vers la face opposée, on parle de déplacement antifacial. Les transformations qui se produisent dans des cercles de petite ou moyenne taille ne peuvent pas entraîner de décalage antéro-facial.
Classes de réarrangements sigmatropiques
[1,3] Les changements
Changements dans les hydrures thermiques
Dans un déplacement thermique [1,3] d'hydrure, un hydrure déplace trois atomes. Les règles de Woodward-Hoffmann stipulent qu'il se déplace dans un mouvement antifacial. Bien qu'un tel déplacement soit autorisé par la symétrie, la topologie de Möbius requise dans l'état de transition interdit un tel déplacement. Il est géométriquement impossible. C'est pourquoi les énols ne s'isomérisent pas sans un catalyseur acide ou basique.
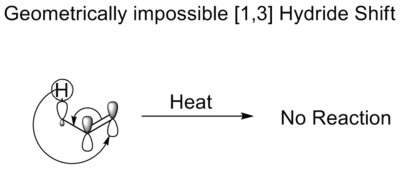
Décalage thermique des alkyles
Les changements d'alkyles thermiques [1,3], similaires aux changements d'hydrures [1,3], doivent se faire de manière antifaciale. La géométrie de l'état de transition est prohibitive. Mais un groupe alkyle, en raison de la nature de ses orbites, peut inverser sa géométrie et former une nouvelle liaison avec le lobe arrière de son orbite sp3. Cette réaction entraînera un déplacement suprafacial. Ces réactions ne sont pas encore courantes dans les systèmes à chaîne ouverte en raison de la nature hautement ordonnée de l'état de transition. Ainsi, les réactions fonctionnent mieux dans les molécules cycliques.
![[1,3] Alkyl Shifts](https://www.alegsaonline.com/image/550px-1,3alkylfixed.png)
Décalages photochimiques [1,3]
Les déplacements photochimiques [1,3] devraient être des déplacements suprafaciaux ; cependant, la plupart ne sont pas préoccupants car ils passent par un état triplet (c'est-à-dire qu'ils ont un mécanisme diradical, auquel les règles de Woodward-Hoffmann ne s'appliquent pas).
[1,5] Les changements
Un déplacement de [1,5] implique le déplacement d'un substituant (-H, -R ou -Ar) vers 5 atomes d'un système π. Il a été démontré que l'hydrogène se déplace dans les systèmes cycliques et à chaîne ouverte à des températures égales ou supérieures à 200 ˚C. On prévoit que ces réactions se déroulent de manière supra-faciale, par un état de transition de Huckel-topologie.
![[1,5] Hydride shift in a cyclic system](https://www.alegsaonline.com/image/300px-1,5hydridecyclicfixed.png)
La photo-irradiation nécessiterait un déplacement antérieur de l'hydrogène. Bien que de telles réactions soient rares, il existe des exemples où les déplacements antarafaciaux sont favorisés :
![Antarafacial [1,5] Hydride Shift](https://www.alegsaonline.com/image/600px-1,5hantarafacialfixed.png)
Contrairement à l'hydrogène [1,5], il n'y a jamais eu de déplacement de l'alkyle [1,5] dans un système à chaîne ouverte. Les chimistes ont déterminé des préférences de taux pour les décalages d'alkyle [1,5] dans les systèmes cycliques : carbonyle et carboxyle> hydrure> phényle et vinyle>> alkyle.
Les groupes alkyles subissent très peu de changements [1,5] et nécessitent généralement des températures élevées. Cependant, pour les cyclohexadiènes, la température des déplacements des alkyles n'est pas beaucoup plus élevée que celle des carbonyles, le meilleur groupe migrateur. Une étude a montré que cela est dû au fait que les déplacements d'alkyle sur les cyclohexadiènes se produisent par un mécanisme différent. D'abord, le cycle s'ouvre, suivi d'un déplacement de [1,7], puis le cycle se reforme de manière électrocyclique :
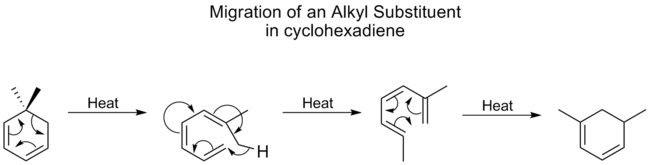
Ce même processus mécaniste est observé ci-dessous, sans la réaction finale de fermeture électrocyclique des anneaux, dans l'interconversion du lumistérol en vitamine D2.
[1,7] Les changements
Les règles de Woodward-Hoffmann prédisent que les changements sigmatropiques se déroulent de manière antifaciale, selon un état de transition topologique de Möbius. Un décalage antarafacial [1,7] est observé dans la conversion du lumistérol en vitamine D2, où, après l'ouverture d'un anneau électrocyclique en prévitamine D2, un méthylhydrogène se déplace.
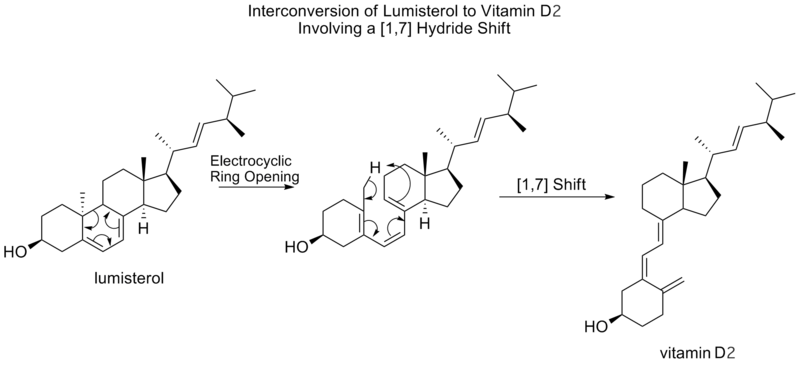
Les non-atriènes bicycliques subissent également des déplacements [1,7] dans un réarrangement dit de marche, qui est le déplacement d'un groupe divalent, comme partie d'un anneau à trois membres, dans une molécule bicyclique.
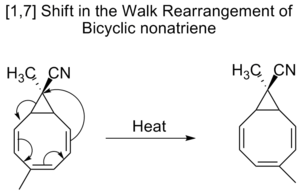
[3,3] Les changements
3,3] Les changements sigmatropiques sont des réarrangements sigmatropiques bien étudiés. Les règles de Woodward-Hoffman prédisent que ces six réactions électroniques se dérouleraient de manière supra-faciale, en utilisant un état de transition topologique de Huckel.
Réorganisation de Claisen
Découvert en 1912 par Rainer Ludwig Claisen, le réarrangement de Claisen est le premier exemple enregistré d'un réarrangement [3,3]-sigmatropique. Ce réarrangement est une réaction utile de formation de liaisons carbone-carbone. Un exemple de réarrangement de Claisen est le réarrangement [3,3] d'un éther allyl-vinylique qui, lorsqu'il est chauffé, donne un carbonyle γ,δ-insaturé. La formation d'un groupe carbonyle rend cette réaction, contrairement à d'autres réarrangements sigmatropiques, intrinsèquement irréversible.

Réarrangement aromatique de Claisen
Le réarrangement ortho-Claisen implique le déplacement [3,3] d'un allylphényléther vers un intermédiaire qui se tautomérise rapidement en un phénol ortho-substitué.
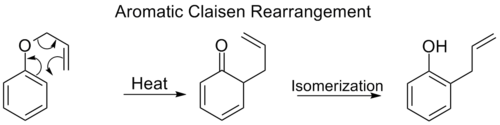
Lorsque les deux positions ortho sur l'anneau benzénique sont bloquées, un deuxième réarrangement ortho-Claisen se produit. Ce réarrangement para-Claisen se termine par la tautomérisation en un phénol tri-substitué.
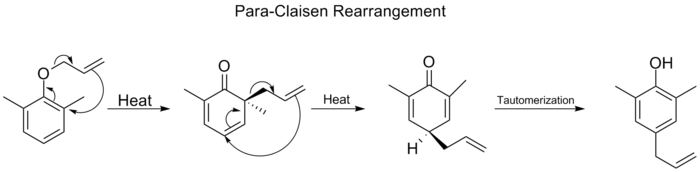
Réorganisation de l'économie
Le réarrangement de Cope est une réaction organique très étudiée impliquant le réarrangement sigmatropique [3,3] des 1,5-diènes. Il a été développé par Arthur C. Cope. Par exemple, le 3,4-diméthyl-1,5-hexadiène chauffé à 300 °C donne du 2,6-octadiène.

Réorganisation de la corde à oxygène
Dans le réarrangement Oxy-Cope, un groupe hydroxyle est ajouté en C3 pour former un énal ou un énone après le tautomérisme céto-énol de l'énol intermédiaire :
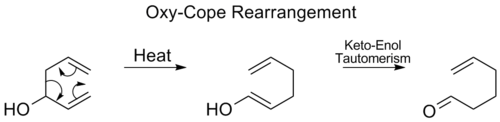
Réorganisation de Carroll
Le réarrangement de Carroll est une réaction de réarrangement en chimie organique et implique la transformation d'un ester d'allyle β-keto en un acide α-allyl-β-ketocarboxylique. Cette réaction organique peut être suivie d'une décarboxylation et le produit final est une γ,δ-allylcétone. Le réarrangement de Carroll est une adaptation du réarrangement de Claisen et constitue effectivement une allylation décarboxylative.
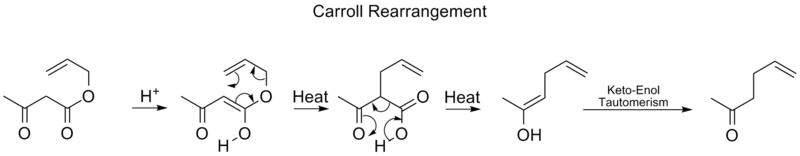
Synthèse de l'indole de Fischer
La synthèse d'indole de Fischer est une réaction chimique qui produit l'indole hétérocyclique aromatique à partir d'une phénylhydrazine (substituée) et d'un aldéhyde ou d'une cétone dans des conditions acides. La réaction a été découverte en 1883 par Hermann Emil Fischer.
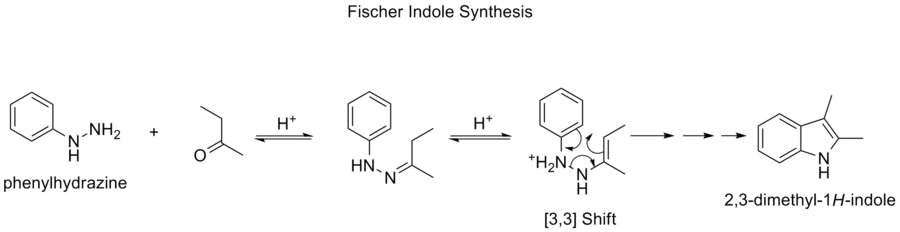
Le choix du catalyseur acide est très important. Parmi les catalyseurs acides qui ont fait leurs preuves, on peut citer Les acides de Bronsted tels que HCl, H2SO4, l'acide polyphosphorique et l'acide p-toluènesulfonique. Les acides de Lewis tels que le trifluorure de bore, le chlorure de zinc, le chlorure de fer et le chlorure d'aluminium sont également des catalyseurs utiles.
Plusieurs revues ont été publiées.
[5,5] Les changements
Comme pour les déplacements [3,3], les règles de Woodward-Hoffman prédisent que les déplacements sigmatropiques [5,5] se dérouleraient de manière supra-faciale, dans l'état de transition topologique de Huckel. Ces réactions sont plus rares que les décalages sigmatropiques [3,3], mais cela est principalement dû au fait que les molécules qui peuvent subir des décalages [5,5] sont plus rares que les molécules qui peuvent subir des décalages [3,3].
![[5,5] shift of phenyl pentadienyl ether](https://www.alegsaonline.com/image/800px-5,5shiftfixeds.png)
Réorganisation de la marche
La migration d'un groupe divalent, tel que O, S, NR ou CR2, qui fait partie d'un anneau à trois membres dans une molécule bicyclique, est communément appelée réarrangement de marche. Selon les règles de Woodward-Hofmann, on peut le caractériser formellement comme étant un déplacement sigmatropique (1, n). Un exemple d'un tel réarrangement est le déplacement des substituants sur les tropilidènes (1,3,5-cycloheptatriènes). Lorsqu'il est chauffé, le système pi passe par un anneau électrocyclique qui se ferme pour former le cycle [4,1,0]heptadiène (norcaradiène). Suivent ensuite un déplacement de [1,5] alkyle et une ouverture de l'anneau électrocyclique.
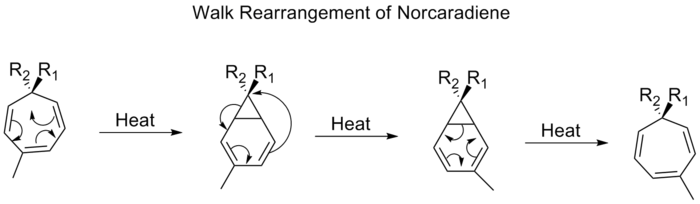
Le réarrangement de la marche des norcaradiènes, qui se fait par une rotation de [1,5], devrait se faire de manière supra-faciale avec conservation de la stéréochimie. Des observations expérimentales montrent cependant que les déplacements de 1,5 des norcaradiens se font de manière antifaciale. Les calculs théoriques ont montré que le déplacement [1,5] est un processus diradical, mais sans impliquer de minima diradicaux sur la surface d'énergie potentielle.
Pages connexes
- Réarrangement 2,3-sigmatropique
- Le changement de NIH
- Théorie orbitale moléculaire de frontière
- Woodward-Hoffmann règne
Questions et réponses
Q : Qu'est-ce qu'une réaction sigmatropique en chimie organique ?
R : Une réaction sigmatropique est une réaction péricyclique qui implique un processus intramoléculaire non catalysé et qui transforme une liaison σ en une autre liaison σ.
Q : Une réaction sigmatropique implique-t-elle un catalyseur ?
R : Une réaction sigmatropique réelle n'implique généralement pas de catalyseur, bien que certaines réactions sigmatropiques puissent être catalysées par un acide de Lewis.
Q : Que signifie le terme "sigmatropique" ?
R : Le terme "sigmatropique" est un mot composé de "sigma", qui fait référence aux liaisons carbone-carbone simples, et du mot grec "tropos", qui signifie tourner.
Q : Quel type de réaction est une réaction sigmatropique ?
R : Une réaction sigmatropique est une réaction de réarrangement, c'est-à-dire que les liaisons d'une molécule se déplacent entre les atomes sans qu'aucun atome ne quitte la molécule ou que de nouveaux atomes ne s'y ajoutent.
Q : Que se passe-t-il dans une réaction sigmatropique intramoléculaire ?
R : Dans une réaction sigmatropique intramoléculaire, un substituant se déplace d'une partie d'un système à liaisons π vers une autre partie, avec réarrangement simultané du système π.
Q : Existe-t-il des réarrangements sigmatropiques bien connus ?
R : Les réarrangements sigmatropiques les plus connus sont le réarrangement de [3,3] Cope, le réarrangement de Claisen, le réarrangement de Carroll et la synthèse de l'indole de Fischer.
Q : Les réactions sigmatropiques font-elles souvent appel à des catalyseurs à base de métaux de transition ?
R : Oui, les réactions sigmatropiques font souvent intervenir des catalyseurs à base de métaux de transition qui forment des intermédiaires dans des réactions analogues.