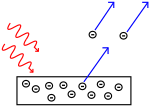
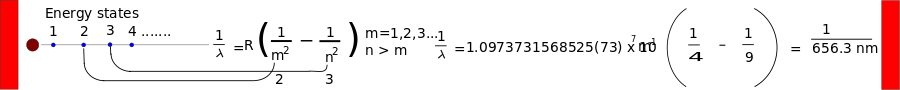Les formules et les idées de la mécanique quantique ont été conçues pour expliquer la lumière qui provient de l'hydrogène incandescent. La théorie quantique de l'atome devait également expliquer pourquoi l'électron reste sur son orbite, ce que d'autres idées n'ont pas pu expliquer. Elle s'inspirait des idées plus anciennes selon lesquelles l'électron devrait tomber au centre de l'atome parce qu'il commence à être maintenu en orbite par sa propre énergie, mais qu'il perdrait rapidement son énergie en tournant sur son orbite. (En effet, on savait que les électrons et autres particules chargées émettaient de la lumière et perdaient de l'énergie lorsqu'ils changeaient de vitesse ou tournaient).
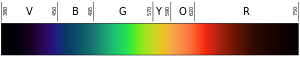
Les lampes à hydrogène fonctionnent comme les néons, mais les néons ont leur propre groupe de couleurs (et fréquences) de lumière. Les scientifiques ont appris qu'ils pouvaient identifier tous les éléments par les couleurs de la lumière qu'ils produisent. Ils n'arrivaient tout simplement pas à comprendre comment les fréquences étaient déterminées.
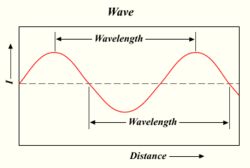
Ensuite, un mathématicien suisse du nom de Johann Balmer a trouvé une équation qui permet de dire ce que serait λ (lambda, pour la longueur d'onde) :
λ = B ( n 2 n 2 - 4 ) n = 3 , 4 , 5 , 6 {\displaystyle \lambda =B\left({\frac {n^{2}}{n^{2}-4}}\right)\qquad \qquad n=3,4,5,6}
où B est un nombre que Balmer a déterminé comme étant égal à 364,56 nm.
Cette équation ne fonctionnait que pour la lumière visible d'une lampe à hydrogène. Mais par la suite, l'équation a été rendue plus générale :
1 λ = R ( 1 m 2 - 1 n 2 ) , {\displaystyle {\frac {1}{\lambda }}=R\left({\frac {1}{m^{2}}}-{\frac {1}{n^{2}}}\right),}
où R est la constante de Rydberg, égale à 0,0110 nm-1, et n doit être supérieur à m.
Si l'on additionne les nombres m et n, il est facile de prédire les fréquences de nombreux types de lumière (ultraviolets, visibles et infrarouges). Pour voir comment cela fonctionne, allez à Hyperphysics et passez au milieu de la page. (Utilisez H = 1 pour l'hydrogène).
En 1908, Walter Ritz a mis au point le principe de combinaison Ritz qui montre comment certains écarts entre les fréquences se répètent sans cesse. Ce principe s'est avéré important pour Werner Heisenberg quelques années plus tard.
En 1905, Albert Einstein a utilisé l'idée de Planck pour montrer qu'un faisceau de lumière est constitué d'un flux de particules appelées photons. L'énergie de chaque photon dépend de sa fréquence. L'idée d'Einstein est le début de l'idée en mécanique quantique que toutes les particules subatomiques comme les électrons, les protons, les neutrons et autres sont à la fois des ondes et des particules. (Voir l'image de l'atome avec l'électron comme ondes à l'atome.) Cela a conduit à une théorie sur les particules subatomiques et les ondes électromagnétiques appelée dualité onde-particule. C'est là que les particules et les ondes n'étaient ni l'une ni l'autre, mais avaient certaines propriétés des deux.
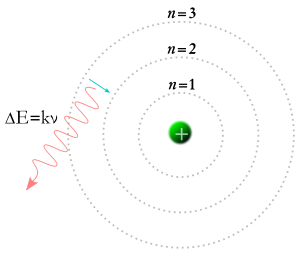
En 1913, Niels Bohr a eu l'idée que les électrons ne pouvaient prendre que certaines orbites autour du noyau d'un atome. Selon la théorie de Bohr, les nombres appelés m et n dans l'équation ci-dessus pourraient représenter des orbites. Selon la théorie de Bohr, les électrons pourraient commencer dans une orbite m et finir dans une orbite n, ou un électron pourrait commencer dans une orbite n et finir dans une orbite m. Ainsi, si un photon frappe un électron, son énergie sera absorbée et l'électron se déplacera vers une orbite plus élevée en raison de cette énergie supplémentaire. Selon la théorie de Bohr, si un électron passe d'une orbite supérieure à une orbite inférieure, il devra alors renoncer à son énergie sous la forme d'un photon. L'énergie du photon sera égale à la différence d'énergie entre les deux orbites, et l'énergie d'un photon lui donne une certaine fréquence et une certaine couleur. La théorie de Bohr a fourni une bonne explication de nombreux aspects des phénomènes subatomiques, mais elle n'a pas réussi à expliquer pourquoi chacune des couleurs de la lumière produite par l'hydrogène incandescent (et par le néon incandescent ou tout autre élément) a une luminosité propre, et les différences de luminosité sont toujours les mêmes pour chaque élément.
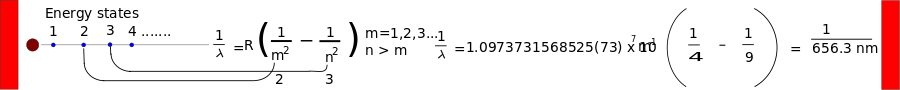
Au moment où Niels Bohr a présenté sa théorie, la plupart des choses sur la lumière produite par une lampe à hydrogène étaient connues, mais les scientifiques ne pouvaient toujours pas expliquer la luminosité de chacune des lignes produites par l'hydrogène incandescent.
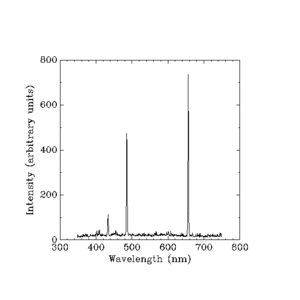
Werner Heisenberg s'est chargé d'expliquer la luminosité ou "l'intensité" de chaque ligne. Il ne pouvait utiliser aucune règle simple comme celle que Balmer avait élaborée. Il a dû utiliser les mathématiques très difficiles de la physique classique qui permettent de tout calculer en termes de choses comme la masse (poids) d'un électron, la charge (force électrique statique) d'un électron et d'autres quantités infimes. La physique classique avait déjà des réponses pour la luminosité des bandes de couleur que produit une lampe à hydrogène, mais la théorie classique disait qu'il devait y avoir un arc-en-ciel continu, et non quatre bandes de couleur séparées. L'explication d'Heisenberg est la suivante :
Il existe une loi qui précise les fréquences de la lumière qui brille de l'hydrogène. Elle doit prédire les fréquences d'espacement lorsque les électrons impliqués se déplacent entre des orbites proches du noyau (centre) de l'atome, mais elle doit également prédire que les fréquences se rapprocheront de plus en plus l'une de l'autre à mesure que nous observerons ce que fait l'électron en se déplaçant entre des orbites de plus en plus éloignées. Il devra également prédire que les différences d'intensité entre les fréquences se rapprochent de plus en plus au fur et à mesure que nous nous éloignons. Là où la physique classique donne déjà les bonnes réponses par un ensemble d'équations, la nouvelle physique doit donner les mêmes réponses mais par des équations différentes.
La physique classique utilise les méthodes du mathématicien français Fourier pour faire une image mathématique du monde physique, et elle utilise des collections de courbes lisses qui vont ensemble pour faire une courbe lisse qui donne, dans ce cas, des intensités pour la lumière de toutes les fréquences à partir d'une certaine lumière. Mais ce n'est pas juste, car cette courbe lisse n'apparaît qu'aux fréquences les plus élevées. Aux fréquences plus basses, il y a toujours des points isolés et rien ne relie les points. Donc, pour faire une carte du monde réel, Heisenberg a dû faire un grand changement. Il a dû faire quelque chose pour ne retenir que les chiffres qui correspondraient à ce que l'on voit dans la nature. On dit parfois qu'il a "deviné" ces équations, mais il ne faisait pas de suppositions aveugles. Il a trouvé ce dont il avait besoin. Les chiffres qu'il a calculés ont permis de mettre des points sur un graphique, mais il n'y a pas eu de ligne tracée entre les points. Et faire un "graphe" uniquement avec des points pour chaque série de calculs aurait fait perdre beaucoup de papier et n'aurait rien donné. Heisenberg a trouvé un moyen de prédire efficacement les intensités pour différentes fréquences et d'organiser ces informations de manière utile.
En utilisant simplement la règle empirique donnée ci-dessus, celle que Balmer a mise en place et que Rydberg a améliorée, nous pouvons voir comment obtenir un ensemble de chiffres qui aiderait Heisenberg à obtenir le type d'image qu'il voulait :
La règle dit que lorsque l'électron passe d'une orbite à l'autre, il gagne ou perd de l'énergie, selon qu'il s'éloigne ou se rapproche du centre. On peut donc placer ces orbites ou ces niveaux d'énergie sous forme de titres en haut et sur le côté d'une grille. Pour des raisons historiques, l'orbite la plus basse est appelée n, et l'orbite suivante est appelée n - a, puis vient n - b, et ainsi de suite. Il est déroutant de constater qu'ils ont utilisé des nombres négatifs alors que les électrons gagnaient en fait de l'énergie, mais c'est bien ainsi.
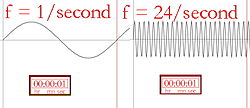
Puisque la règle de Rydberg nous donne des fréquences, nous pouvons utiliser cette règle pour mettre des nombres en fonction de l'endroit où va l'électron. Si l'électron commence à n et finit à n, alors il n'est pas vraiment allé quelque part, donc il n'a pas gagné d'énergie et il n'en a pas perdu. La fréquence est donc de 0. Si l'électron commence à n-a et finit à n, alors il est passé d'une orbite supérieure à une orbite inférieure. Dans ce cas, il perd de l'énergie, et l'énergie qu'il perd se présente sous la forme d'un photon. Le photon a une certaine quantité d'énergie, e, et cela est lié à une certaine fréquence f par l'équation e = h f. Nous savons donc qu'un certain changement d'orbite va produire une certaine fréquence de lumière, f. Si l'électron commence à n et finit à n - a, cela signifie qu'il est passé d'une orbite inférieure à une orbite supérieure. Cela ne se produit que lorsqu'un photon d'une certaine fréquence et d'une certaine énergie arrive de l'extérieur, est absorbé par l'électron et lui donne son énergie, et c'est ce qui fait que l'électron sort vers une orbite plus élevée. Donc, pour que tout ait un sens, nous écrivons cette fréquence comme un nombre négatif. Il y avait un photon avec une certaine fréquence et maintenant il a été enlevé.
On peut donc faire une grille comme celle-ci, où f(a←b) signifie la fréquence impliquée lorsqu'un électron passe de l'état d'énergie (orbite) b à l'état d'énergie a (Là encore, les séquences sont rétrospectives, mais c'est ainsi qu'elles ont été écrites à l'origine) :
Grille de f
| États d'électrons | n | n-a | n-b | n-c | .... | |
| n | f(n←n) | f(n←n-a) | f(n←n-b) | f(n←n-c) | ..... | |
| n-a | f(n-a←n) | f(n-a←n-a) | f(n-a←n-b) | f(n-a←n-c) | ..... | |
| n-b | f(n-b←n) | f(n-b←n-a) | f(n-b←n-b) | f(n-b←n-c) | ..... | |
| transition.... | ..... | ..... | ..... | ..... | | |
Heisenberg n'a pas fait les grilles comme cela. Il a juste fait le calcul qui lui permettrait d'obtenir les intensités qu'il recherchait. Mais pour ce faire, il a dû multiplier deux amplitudes (la hauteur d'une onde) pour calculer l'intensité. (En physique classique, l'intensité est égale à l'amplitude au carré.) Il a fait une équation étrange pour résoudre ce problème, a rédigé le reste de son papier, l'a remis à son patron et est parti en vacances. Le Dr. Born a regardé sa drôle d'équation et elle lui a paru un peu folle. Il a dû se demander : "Pourquoi Heisenberg m'a-t-il donné cette chose étrange ? Pourquoi doit-il le faire de cette façon ?" Puis il a réalisé qu'il cherchait un plan pour quelque chose qu'il connaissait déjà très bien. Il avait l'habitude d'appeler la grille ou le tableau que nous pouvions écrire en faisant, par exemple, tous les calculs pour les fréquences, une matrice. Et l'étrange équation d'Heisenberg était une règle pour multiplier deux d'entre elles ensemble. Max Born était un très, très bon mathématicien. Il savait que puisque les deux matrices (grilles) multipliées représentent des choses différentes (comme la position (x,y,z) et la quantité de mouvement (mv), par exemple), alors quand vous multipliez la première matrice par la seconde, vous obtenez une réponse et quand vous multipliez la seconde matrice par la première, vous obtenez une autre réponse. Même s'il ne connaissait pas les matrices mathématiques, Heisenberg voyait déjà ce problème de "réponses différentes" et cela l'avait dérangé. Mais le Dr. Born était un si bon mathématicien qu'il a vu que la différence entre la première multiplication de la matrice et la deuxième multiplication de la matrice allait toujours impliquer la constante de Planck, h, multipliée par la racine carrée de l'unité négative, i. Donc, quelques jours après la découverte de Heisenberg, ils avaient déjà les bases mathématiques de ce que Heisenberg aimait appeler le "principe d'indétermination". Par "indéterminé", Heisenberg voulait dire que quelque chose comme un électron n'est pas immobilisé tant qu'il n'est pas immobilisé. C'est un peu comme une méduse qui est toujours en train de s'écraser et qui ne peut pas être "à un endroit" à moins que vous ne la tuiez. Plus tard, les gens ont pris l'habitude de l'appeler "le principe d'incertitude d'Heisenberg", ce qui a fait commettre à beaucoup l'erreur de penser que les électrons et les choses de ce genre sont vraiment "quelque part" mais que nous en sommes simplement incertains dans notre propre esprit. Cette idée est fausse. Ce n'est pas ce dont Heisenberg parlait. Avoir du mal à mesurer quelque chose est un problème, mais ce n'est pas le problème dont Heisenberg parlait.
L'idée d'Heisenberg est très difficile à saisir, mais nous pouvons la rendre plus claire avec un exemple. Tout d'abord, nous commencerons à appeler ces grilles "matrices", car nous devrons bientôt parler de multiplication des matrices.
Supposons que nous commencions avec deux types de mesures, la position (q) et l'élan (p). En 1925, Heisenberg a écrit une équation comme celle-ci :
Y ( n , n - b ) = ∑ a p ( n , n - a ) q ( n - a , n - b ) {\displaystyle Y(n,n-b)=\sum _{a}^{}\,p(n,n-a)q(n-a,n-b)} (Equation pour les variables conjuguées élan et position)
(Equation pour les variables conjuguées élan et position)
Il ne le savait pas, mais cette équation donne un plan pour écrire deux matrices (grilles) et pour les multiplier. Les règles pour multiplier une matrice par une autre sont un peu compliquées, mais voici les deux matrices selon le plan, puis leur produit :
Matrice de p
| États d'électrons | n-a | n-b | n-c | .... | |
| n | p(n←n-a) | p(n←n-b) | p(n←n-c) | ..... | |
| n-a | p(n-a←n-a) | p(n-a←n-b) | p(n-a←n-c) | ..... | |
| n-b | p(n-b←n-a) | p(n-b←n-b) | p(n-b←n-c) | ..... | |
| transition.... | ..... | ..... | ..... | ..... | |
Matrice de q
| États d'électrons | n-b | n-c | n-d | .... | |
| n-a | q(n-a←n-b) | q(n-a←n-c) | q(n-a←n-d) | ..... | |
| n-b | q(n-b←n-b) | q(n-b←n-c) | q(n-b←n-d) | ..... | |
| n-c | q(n-c←n-b) | q(n-c←n-c) | q(n-c←n-d) | ..... | |
| transition.... | ..... | ..... | ..... | ..... | |
La matrice du produit des deux matrices ci-dessus, telle que spécifiée par l'équation pertinente dans l'article de Heisenberg de 1925, est la suivante
| États d'électrons | n-b | n-c | n-d | ..... |
| n | A | ..... | ..... | ..... |
| n-a | ..... | B | ..... | ..... |
| n-b | ..... | ..... | C | ..... |
Où :
A=p(n←n-a)*q(n-a←n-b)+p(n←n-b)*q(n-b←n-b)+p(n←n-c)*q(n-c←n-b)+.....
B=p(n-a←n-a)*q(n-a←n-c)+p(n-a←n-b)*q(n-b←n-c)+p(n-a←n-c)*q(n-c←n-c)+.....
C=p(n-b←n-a)*q(n-a←n-d)+p(n-b←n-b)*q(n-b←n-d)+p(n-b←n-c)*q(n-d←n-d)+.....
et ainsi de suite.
Si les matrices étaient inversées, les valeurs suivantes en résulteraient :
A=q(n←n-a)*p(n-a←n-b)+q(n←n-b)*p(n-b←n-b)+q(n←n-c)*p(n-c←n-b).....+
B=q(n-a←n-a)*p(n-a←n-c)+q(n-a←n-b)*p(n-b←n-c)+q(n-a←n-c)*p(n-c←n-c).....+
C=q(n-b←n-a)*p(n-a←n-d)+q(n-b←n-b)*p(n-b←n-d)+q(n-b←n-c)*p(n-d←n-d)+.....
et ainsi de suite.
Notez comment le changement de l'ordre de multiplication modifie les nombres, pas à pas, qui sont effectivement multipliés.