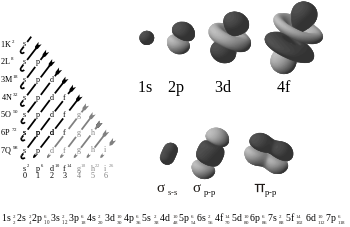
En chimie, les liaisons pi (π bonds) sont des liaisons chimiques covalentes où le chemin orbital d'un électron croise (chevauche) le chemin d'un autre. Les électrons ont un lobe en forme de huit (voir photo). Il y a deux zones de chevauchement car les trajectoires se chevauchent sur les deux lobes. Un seul des plans nodaux de l'orbite passe par les deux noyaux concernés.
La lettre grecque π dans leur nom fait référence aux p orbitales. La symétrie orbitale de la liaison pi est identique à celle de l'orbitale p lorsqu'elle est vue sur l'axe de la liaison. Les p orbitales ont généralement ce type de liaison. Les orbitales D sont également supposées utiliser le lien pi, mais ce n'est pas nécessairement ce qui se passe dans la réalité. L'idée de lier les orbitales d s'inscrit dans la théorie de l'hypervalence.
Les obligations Pi sont généralement plus faibles que les obligations sigma. Selon la mécanique quantique, cela s'explique par le fait que les trajectoires orbitales sont parallèles et qu'il y a donc beaucoup moins de chevauchement entre les p-orbitales.
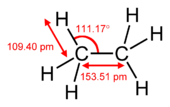
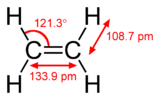
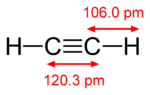
Les liaisons Pi se produisent lorsque deux orbitales atomiques sont en contact à travers deux zones de chevauchement. Les liaisons Pi sont des liaisons plus étalées que les liaisons sigma. Les électrons des liaisons pi sont parfois appelés électrons pi. Les fragments moléculaires reliés par une liaison pi ne peuvent pas tourner autour de cette liaison sans rompre la liaison pi. La rotation détruit les trajectoires parallèles des deux p orbitales.