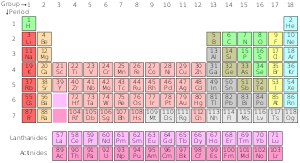
Le tableau périodique des éléments chimiques est une liste des éléments chimiques connus. Dans le tableau, les éléments sont placés dans l'ordre de leur numéro atomique en commençant par le plus petit nombre de un, l'hydrogène. Le numéro atomique d'un élément est le même que le nombre de protons dans ce noyau particulier d'un atome. Dans le tableau périodique, les éléments sont disposés en périodes et en groupes. Une rangée d'éléments dans le tableau est appelée un point. Chaque période a un numéro ; de 1 à 8. La période 1 ne contient que deux éléments : l'hydrogène et l'hélium. La période 2 et la période 3 ont toutes deux 8 éléments. Les autres périodes sont plus longues. Les éléments d'un point ont des numéros atomiques consécutifs.
Une colonne d'éléments en bas du tableau est appelée un groupe. Il y a 18 groupes dans le tableau périodique standard. Chaque groupe a un numéro : de 1 à 18. Les éléments d'un groupe ont des électrons disposés de manière similaire, selon le nombre d'électrons de valence, ce qui leur donne des propriétés chimiques similaires (ils se comportent de manière similaire). Par exemple, le groupe 18 est connu sous le nom de "gaz rares" parce qu'ils sont tous des gaz et qu'ils ne se combinent pas avec d'autres atomes.
Il existe deux systèmes de numéros de groupe, l'un utilisant des chiffres arabes (1,2,3) et l'autre des chiffres romains (I, II, III). Les noms en chiffres romains ont été utilisés pendant la plus grande partie du 20e siècle. En 1990, l'Union internationale de chimie pure et appliquée (UICPA) a décidé d'utiliser le nouveau système avec des chiffres arabes, pour remplacer les deux anciens systèmes de groupes qui utilisaient des chiffres romains.
Le tableau périodique a été utilisé par les chimistes pour observer les modèles et les relations entre les éléments. Le tableau périodique comprend trois groupes principaux : les métaux, les métalloïdes et les non-métaux. Par exemple, les éléments en bas et à l'extrême gauche du tableau sont les plus métalliques, et les éléments en haut à droite sont les moins métalliques. (par exemple, le césium est beaucoup plus métallique que l'hélium). Il existe également de nombreux autres motifs et relations.
Le tableau périodique a été inventé par le chimiste russe Dmitry Ivanovich Mendeleyev (1834-1907). En son honneur, l'élément 101 a été nommé en son honneur, le mendélévium.