Les anions tels que Cl-, ou un composé avec une paire d'électrons isolés tel que NH3 (ammoniac) sont des exemples de nucléophiles.
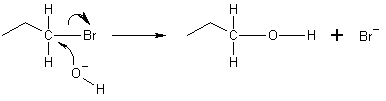
Dans l'exemple ci-dessous, l'oxygène de l'ion hydroxyde donne une paire d'électrons pour se lier au carbone à l'extrémité de la molécule de bromopropane. La liaison entre le carbone et le brome subit ensuite une fission hétérolytique, l'atome de brome prenant l'électron donné et devenant l'ion bromure (Br-). Il s'agit d'une réaction SN2 qui se produit par attaque à l'envers. Cela signifie que l'ion hydroxyde attaque l'atome de carbone de l'autre côté, exactement à l'opposé de l'ion brome. En raison de cette attaque par l'arrière, les réactions SN2 entraînent une inversion de la configuration de l'électrophile. Si l'électrophile est chiral, il conserve généralement sa chiralité, bien que la configuration du produit SN2 soit inversée par rapport à celle de l'électrophile d'origine (inversion de Walden).
Un nucléophile ambiant est un nucléophile qui peut attaquer à partir de deux ou plusieurs endroits, ce qui donne deux ou plusieurs produits. Par exemple, l'ion thiocyanate (SCN-) peut attaquer soit le S soit le N. Pour cette raison, la réaction SN2 d'un halogénure d'alkyle avec le SCN- conduit souvent à un mélange de RSCN (un thiocyanate d'alkyle) et de RNCS (un isothiocyanate d'alkyle). Des mélanges similaires se produiront dans la synthèse des nitriles de Kolbe.
Nucléophiles de carbone
Les halogénures de métaux alkyles sont des nucléophiles de carbone que l'on trouve dans la réaction de Grignard, la réaction de Blaise, la réaction de Reformatsky et la réaction de Barbier, des réactifs organolithiques et des anions d'un alcyne terminal.
Les énols sont également des nucléophiles du carbone. La formation d'un énol est catalysée par un acide ou une base. Les énols sont des nucléophiles ambides, mais en général, ils sont nucléophiles au niveau de l'atome de carbone à côté des carbones à double liaison (atome de carbone alpha). Les énols sont couramment utilisés dans les réactions de condensation, notamment la condensation de Claisen et les réactions de condensation des aldols.
Nucléophiles de l'oxygène
Les nucléophiles de l'oxygène sont par exemple l'eau (H2O), l'anion hydroxyde, les alcools, les anions alcoxydes, le peroxyde d'hydrogène et les anions carboxylates.
Nucléophiles du soufre
Parmi les nucléophiles soufrés, le sulfure d'hydrogène et ses sels, les thiols (RSH), les anions thiolates (RS-), les anions des acides thiolcarboxyliques (RC(O)-S-), et les anions des dithiocarbonates (RO-C(S)-S-) et des dithiocarbamates (R2N-C(S)-S-) sont les plus utilisés.
En général, le soufre est très nucléophile en raison de sa grande taille, qui le rend facilement polarisable, et ses paires d'électrons isolés sont facilement accessibles.
Les nucléophiles de l'azote
Les nucléophiles de l'azote comprennent l'ammoniac, l'azide, les amines et les nitrites.
