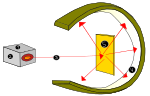
En 1850, Sir William Crookes a construit un "tube à décharge", c'est-à-dire un tube en verre dont l'air est évacué et dont les extrémités sont munies d'électrodes métalliques, relié à une source de haute tension. En créant un vide dans le tube, on peut observer une légère décharge qui va de la cathode (électrode chargée négativement) à l'anode (électrode chargée positivement). Les escrocs ont baptisé cette émission "rayons cathodiques".
Après les expériences sur les rayons cathodiques, Sir Joseph John Thomson a établi que le rayon émis était formé par des charges négatives, parce qu'elles étaient attirées par le pôle positif. Thomson savait que les atomes étaient électriquement neutres, mais il a établi que, pour que cela se produise, un atome devait avoir la même quantité de charges négatives et positives. Les charges négatives ont été appelées électrons (e-).
Selon les hypothèses établies sur la charge neutre des atomes, Thomson a proposé le premier modèle atomique, décrit comme une sphère chargée positivement dans laquelle les électrons sont incrustés (avec des charges négatives). Ce modèle est connu sous le nom de modèle du plum-pudding.
En 1906, Robert Millikan a déterminé que les électrons avaient une charge de Coulomb (C) de -1,6 * 10-19, ce qui permettait de calculer sa masse comme étant minuscule, égale à 9,109 * 10-31 kg.
Dans le même temps, les expériences menées par Eugene Goldstein en 1886 avec des tubes à décharge cathodique lui ont permis d'établir que les charges positives avaient une masse de 1,6726 * 10-27 kg et une charge électrique de +1,6 * 10 -19 C. Lord Ernest Rutherford a ensuite nommé ces particules chargées positivement des protons