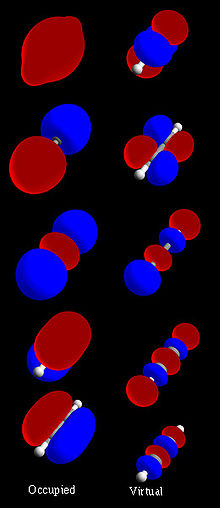
Les chimistes doivent comprendre la géométrie des MO afin de pouvoir discuter de la structure moléculaire. La méthode LCMO (Linear combination of atomic orbitals molecular orbital) donne une description grossière mais correcte des MO. Dans cette méthode, les orbitales moléculaires sont exprimées comme des combinaisons linéaires de toutes les orbitales atomiques de chaque atome de la molécule.
Combinaisons linéaires d'orbitales atomiques (LCAO)
Les orbites moléculaires ont été introduites pour la première fois par Friedrich Hund et Robert S. Mulliken en 1927 et 1928.
La combinaison linéaire des orbitales atomiques ou approximation "LCAO" pour les orbitales moléculaires a été introduite en 1929 par Sir John Lennard-Jones. Son article révolutionnaire a montré comment dériver la structure électronique des molécules de fluor et d'oxygène à partir de principes quantiques. Cette approche qualitative de la théorie des orbitales moléculaires fait partie des débuts de la chimie quantique moderne.
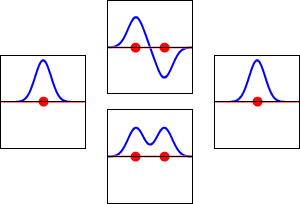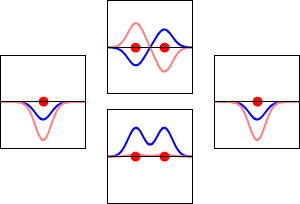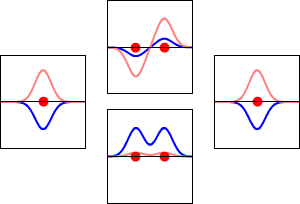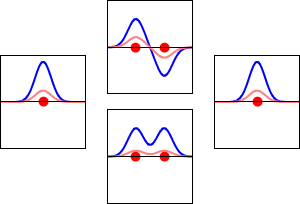
Les combinaisons linéaires d'orbitales atomiques (LCAO) peuvent être utilisées pour deviner les orbitales moléculaires qui se forment lorsque les atomes de la molécule se lient entre eux. Comme pour une orbitale atomique, une équation de Schrodinger, qui décrit le comportement d'un électron, peut également être construite pour une orbitale moléculaire. Les combinaisons linéaires des orbitales atomiques (les sommes et les différences des fonctions d'onde atomique) fournissent des solutions approximatives aux équations moléculaires de Schrodinger. Pour les molécules diatomiques simples, les fonctions d'onde que vous obtenez sont représentées mathématiquement par les équations
Ψ = caψa + cbψb
et
Ψ* = caψa - cbψb
où Ψ et Ψ* sont les fonctions d'ondes moléculaires pour les orbitales moléculaires de liaison et d'anti-liaison, respectivement, ψa et ψb sont les fonctions d'ondes atomiques des atomes a et b, respectivement, et ca et cb sont des coefficients ajustables. Ces coefficients peuvent être positifs ou négatifs, selon les énergies et les symétries des orbitales atomiques individuelles. Lorsque les deux atomes se rapprochent, leurs orbitales atomiques se chevauchent pour produire des zones de haute densité d'électrons. Ainsi, des orbitales moléculaires se forment entre les deux atomes. Les atomes sont maintenus ensemble par l'attraction électrostatique entre les noyaux chargés positivement et les électrons chargés négativement qui occupent les orbitales moléculaires de liaison.
Les modes opératoires de cautionnement, d'anti-recordement et de non-recordement
Lorsque les orbitales atomiques interagissent, l'orbite moléculaire qui en résulte peut être de trois types : liante, anti-liante ou non-liante.
L'établissement de liens entre les modes opératoires :
- Les interactions de liaison entre les orbitales atomiques sont des interactions constructives (en phase).
- Les MO de liaison ont une énergie plus faible que les orbites atomiques qui se combinent pour les produire.
Les modes opératoires anti-liaison :
- Les interactions anti-liaison entre les orbitales atomiques sont des interactions destructrices (déphasées).
- Les MO anti-liaison ont une énergie plus élevée que les orbites atomiques qui se combinent pour les produire.
Les modes opératoires non contraignants :
- Les MO non liés sont le résultat d'une absence d'interaction entre les orbitales atomiques en raison de l'absence de symétries compatibles.
- Les MO non liés auront la même énergie que les orbitales atomiques de l'un des atomes de la molécule.
HOMO et LUMO
Chaque orbite moléculaire a son propre niveau d'énergie. Les chimistes trient les MO par niveau d'énergie. Les chimistes partent du principe que les électrons rempliront en premier les MO de plus faible niveau d'énergie. Par exemple, si une molécule a des électrons pour remplir 15 orbitales, les 15 MO ayant les niveaux d'énergie les plus bas seront remplis. La 15e MO de la liste serait appelée "orbitale moléculaire la plus occupée" (HOMO) et la 16e MO de la liste serait appelée "orbitale moléculaire inoccupée la plus basse" (LUMO). La différence entre le niveau d'énergie de la HOMO et celui de la LUMO s'appelle la bande interdite. La bande interdite peut parfois servir de mesure de l'excitabilité de la molécule : plus l'énergie est faible, plus elle sera facilement excitée. Lorsque l'électron est excité, il sautera vers un MO inoccupé. Cela peut par exemple aider à deviner si quelque chose va émettre de la lumière (luminescence).