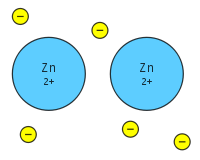
Une liaison métallique est le partage de nombreux électrons détachés entre de nombreux ions positifs, où les électrons agissent comme une "colle" donnant à la substance une structure définie. Elle est différente de la liaison covalente ou ionique. Les métaux ont une faible énergie d'ionisation. Par conséquent, les électrons de valence peuvent être délocalisés à travers les métaux. Les électrons délocalisés ne sont pas associés à un noyau particulier d'un métal, ils sont plutôt libres de se déplacer dans toute la structure cristalline en formant une "mer" d'électrons.
Les électrons et les ions positifs du métal ont une forte force d'attraction entre eux. C'est pourquoi les métaux ont souvent un point de fusion ou d'ébullition élevé. Le principe est similaire à celui des liaisons ioniques.
Les liaisons métalliques sont à l'origine de nombreuses caractéristiques des métaux, telles que la résistance, la malléabilité, la ductilité, le lustre, la conduction de la chaleur et de l'électricité.
Comme les électrons se déplacent librement, le métal a une certaine conductivité électrique. Il permet à l'énergie de passer rapidement à travers les électrons, générant ainsi un courant électrique. Les métaux conduisent la chaleur pour la même raison : les électrons libres peuvent transférer l'énergie à un rythme plus rapide que d'autres substances dont les électrons sont fixés en position. Il existe également peu de substances non métalliques qui conduisent l'électricité : le graphite (car, comme les métaux, il possède des électrons libres) et les composés ioniques qui sont fondus ou dissous dans l'eau, qui possèdent des ions libres en mouvement.
Les liaisons métalliques ont au moins un électron de valence qu'elles ne partagent pas avec les atomes voisins, et elles ne perdent pas d'électrons pour former des ions. Au contraire, les niveaux d'énergie extérieurs (orbitales atomiques) des atomes de métal se chevauchent. Ils sont similaires aux liaisons covalentes. Tous les métaux ne présentent pas de liaison métallique. Par exemple, les ions de mercure (Hg2+
2) forment des liaisons covalentes métal-métal.
Un alliage est une solution de métaux. La plupart des alliages sont brillants comme le sont les métaux purs.