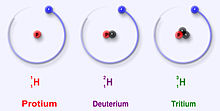
L'hydrogène a trois isotopes principaux : le protium (1H), le deutérium (2H) et le tritium (3H). Ces isotopes se forment naturellement dans la nature. Le protium et le deutérium sont stables. Le tritium est radioactif et a une demi-vie d'environ 12 ans. Les scientifiques ont créé quatre autres isotopes de l'hydrogène (4H à 7H), mais ces isotopes sont très instables et n'existent pas dans la nature.
Les principaux isotopes de l'hydrogène sont uniques car ils sont les seuls à avoir un nom. Ces noms sont encore utilisés aujourd'hui. Le deutérium et le tritium ont parfois leurs propres symboles, D et T. Cependant, l'Union internationale de chimie pure et appliquée n'aime pas beaucoup ces noms, même s'ils sont souvent utilisés. D'autres isotopes avaient leur propre nom lorsque les scientifiques étudiaient la radioactivité. Mais, leurs noms ne sont plus utilisés aujourd'hui.