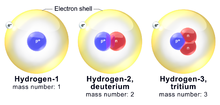
Les atomes d'un élément chimique peuvent exister sous différentes formes. On les appelle des isotopes. Ils ont le même nombre de protons (et d'électrons), mais un nombre différent de neutrons. Les différents isotopes d'un même élément ont des masses différentes. La masse est le mot qui désigne la quantité de substance (ou de matière) que possède un élément. Les objets de masse différente ont des poids différents. Comme les différents isotopes ont des nombres de neutrons différents, ils n'ont pas tous le même poids ou la même masse.
Les différents isotopes d'un même élément ont le même numéro atomique. Ils ont le même nombre de protons. Le numéro atomique est déterminé par le nombre de protons. Les isotopes ont cependant des nombres de masse différents, car ils ont des nombres de neutrons différents.
Le mot "isotope", qui signifie "au même endroit", vient du fait que les isotopes sont au même endroit sur le tableau périodique.
Dans un atome neutre, le nombre d'électrons est égal au nombre de protons. Les isotopes d'un même élément ont également le même nombre d'électrons et la même structure électronique. Comme la façon dont un atome agit est déterminée par sa structure électronique, les isotopes sont presque identiques chimiquement, mais différents physiquement de leurs atomes d'origine.
Les isotopes plus lourds réagissent chimiquement plus lentement que les isotopes plus légers du même élément. Cet "effet de masse" est plus important pour le protium (1H) et le deutérium (2H), car le deutérium a deux fois la masse du protium. Pour les éléments plus lourds, le rapport de poids atomique relatif entre les isotopes est beaucoup plus faible, et l'effet de masse est généralement faible.