Réaction de Grignard
La réaction de Grignard (prononcée /ɡriɲar) est une réaction chimique organométallique dans laquelle les halogénures d'alkyl- ou d'aryl-magnésium (réactifs de Grignard) attaquent les atomes de carbone électrophiles qui sont présents dans les liaisons polaires (par exemple, dans un groupe carbonyle comme dans l'exemple ci-dessous). Les réactifs de Grignard agissent comme des nucléophiles. La réaction de Grignard produit une liaison carbone-carbone. Elle modifie l'hybridation autour du centre de la réaction. La réaction de Grignard est un outil important dans la formation des liaisons carbone-carbone. Elle peut également former des liaisons carbone-phosphore, carbone-étain, carbone-silicium, carbone-bore et autres liaisons carbone-hétéroatomes.
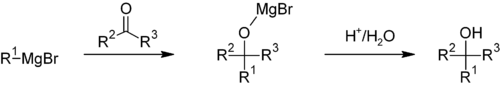
Il s'agit d'une réaction d'addition organométallique nucléophile. La valeur élevée du pKa du composant alkyle (pKa = ~45) rend la réaction irréversible. Les réactions de Grignard ne sont pas ioniques. Le réactif de Grignard existe sous la forme d'un amas organométallique (dans l'éther).
L'inconvénient des réactifs de Grignard est qu'ils réagissent facilement avec des solvants protiques (comme l'eau), ou avec des groupes fonctionnels contenant des protons acides, comme les alcools et les amines. L'humidité atmosphérique peut modifier le rendement de la fabrication d'un réactif de Grignard à partir de tournures de magnésium et d'un halogénure d'alkyle. Une des nombreuses méthodes utilisées pour exclure l'eau de l'atmosphère de réaction consiste à sécher à la flamme le récipient de réaction pour évaporer toute l'humidité, qui est ensuite scellée pour empêcher le retour de l'humidité. Les chimistes utilisent ensuite des ultrasons pour activer la surface du magnésium afin qu'il consomme toute l'eau présente. Cela peut permettre aux réactifs de Grignard de se former avec une sensibilité moindre à la présence d'eau.
Un autre inconvénient des réactifs de Grignard est qu'ils ne forment pas facilement des liaisons carbone-carbone en réagissant avec les halogénures d'alkyle par un mécanisme SN2.
François Auguste Victor Grignard a découvert les réactions et les réactifs de Grignard. Ils portent le nom de ce chimiste français (Université de Nancy, France) qui a reçu le prix Nobel de chimie en 1912 pour ces travaux.
Questions et réponses
Q : Qu'est-ce que la réaction de Grignard ?
R : La réaction de Grignard est une réaction chimique organométallique dans laquelle des halogénures d'alkyl- ou d'aryl-magnésium (réactifs de Grignard) attaquent des atomes de carbone électrophiles présents dans des liaisons polaires.
Q : Quel type de liaison la réaction de Grignard produit-elle ?
R : La réaction de Grignard produit une liaison carbone-carbone.
Q : Quels autres types de liaisons peuvent être formés à l'aide de la réaction de Grignard ?
R : La réaction de Grignard peut également former des liaisons carbone-phosphore, carbone-étain, carbone-silicium, carbone-bore et d'autres liaisons carbone-hétéroatome.
Q : Comment la valeur élevée du pKa du composant alkyle affecte-t-elle la réaction de Grignard ?
R : La valeur élevée du pKa du composant alkyle (pKa = ~45) rend la réaction irréversible.
Q : Dans quel type de réactions d'addition les réactifs de Grignard interviennent-ils ?
R : Les réactifs de Grignard prennent part à des réactions d'addition organométalliques nucléophiles.
Q : Quels sont les inconvénients liés à l'utilisation des réactifs de Grignard ? R : Parmi les inconvénients associés à l'utilisation des réactifs de Grignard, citons leur réactivité avec les solvants protiques tels que l'eau et les groupes fonctionnels à protons acides, tels que les alcools et les amines ; la sensibilité à l'humidité atmosphérique ; et la difficulté à former des liaisons carbone-carbone en réagissant avec des halogénures d'alkyle par un mécanisme SN2.
Q : Qui a découvert la réaction de Grigand et ses réactifs ?
R : La découverte de la réaction et du réactif de Griand est attribuée au chimiste français Franחois Auguste Victor Griand qui a reçu le prix Nobel de chimie en 1912 pour ce travail.
Rechercher dans l'encyclopédie