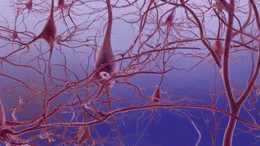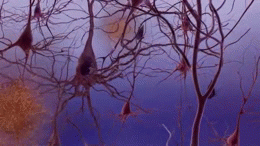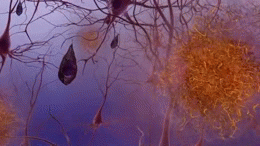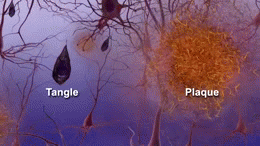
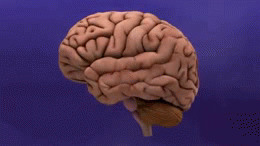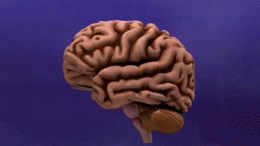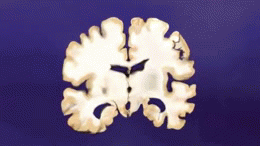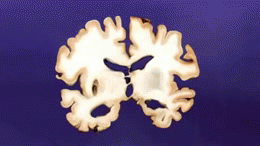
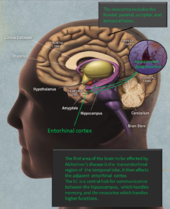
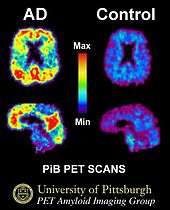
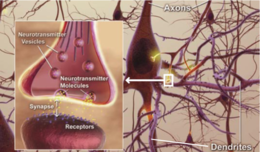
Deux des principales caractéristiques du cerveau des personnes atteintes de la maladie d'Alzheimer sont les enchevêtrements neurobrillaires ("tangles" en abrégé), qui sont constitués d'une protéine appelée tau, et les plaques séniles (qui sont principalement constituées d'une autre protéine appelée bêta-amyloïde, elles sont aussi parfois appelées faisceaux bêta-amyloïdes ou "bundles" en abrégé). Les protéines tau qui forment les enchevêtrements maintenaient auparavant ensemble une structure à l'intérieur des neurones appelée microtubule qui est une partie importante du neurone ; elle fait partie du cytosquelette (squelette cellulaire) qui est ce qui maintient la forme d'une cellule, et les microtubules jouent un rôle dans la communication cellulaire.
Les enchevêtrements et les plaques peuvent être causés par d'autres maladies, comme le virus Herpes simplex de type 1 qui est étudié comme cause ou facteur possible du développement de la maladie d'Alzheimer. On ne sait pas avec certitude si les enchevêtrements et les plaques font partie des causes de la maladie d'Alzheimer ou s'ils en sont les résultats.
Microtubules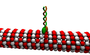
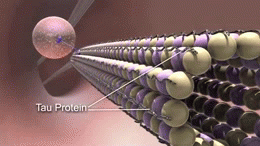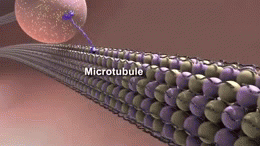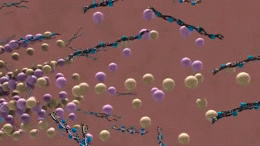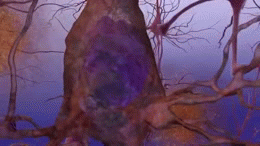
Les microtubules sont constitués d'une protéine appelée tubuline. La tubuline est polymérisée, c'est-à-dire que les molécules forment sans cesse des formes identiques qui sont reliées entre elles en groupes, et ces groupes sont reliés entre eux. Ils peuvent former de longues chaînes ou d'autres formes ; dans ce cas, la tubuline polymérisée forme des microtubules. Les microtubules sont des tubes rigides comme des pailles microscopiques qui sont creux à l'intérieur. Les microtubules aident à conserver la forme du neurone et sont impliqués dans le passage des signaux à travers le neurone.
Tau
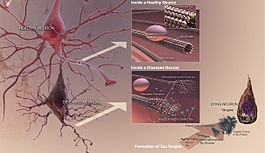
La Tau est une protéine que l'on trouve principalement dans les neurones du système nerveux central. Elles aident à maintenir les microtubules ensemble dans les neurones. Et lorsque des changements se produisent dans la façon dont les protéines tau sont censées fonctionner, les microtubules se brisent. Les protéines tau qui ne maintiennent plus les microtubules ensemble forment des brins appelés fibrilles, qui s'agglutinent ensuite à l'intérieur du neurone pour former ce qu'on appelle des enchevêtrements neurofibrillaires. Ces amas, également appelés "enchevêtrements tau", sont tout ce qui reste après la mort d'un neurone.
| Stade de braquage des modifications neurofibrillaires liées à la maladie d'Alzheimer.
Cette méthode est actuellement utilisée uniquement à des fins de recherche |
| Scène | Les neurofibrillaires s'emmêlent : | Symptômes |
|
I/IIStage transentorhinal
| Région transentorhinale et région entorhinale | Aucun symptôme |
|
III/IVStade limbique
| Formation de l'hippocampe et de certaines parties du système limbique et de l'amygdale | Début de la maladie d'
AlzheimerDéficiences cognitives
: problèmes de mémoire, cognition spatiale |
| V/VIIétape critique | Dans tout le cortex cérébral | Démence : maladie d'Alzheimer en plein développement |
Bêta-amyloïde
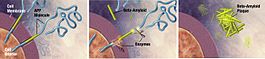
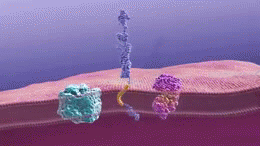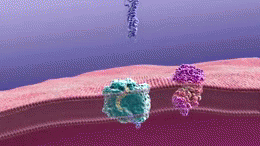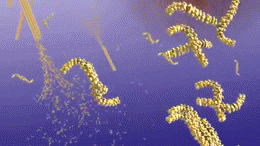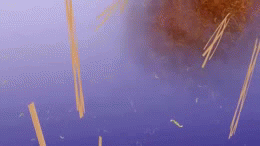
Les plaques de bêta-amyloïde (Aβ) (également appelée "bêta-amyloïde") commencent par une protéine appelée protéine précurseur amyloïde (APP). L'APP est l'une des protéines qui composent la membrane ou le revêtement extérieur d'une cellule, qui protège la cellule. Dans ce cas, un neurone.. Comme elle est fabriquée à l'intérieur de la cellule, l'APP sort à travers la membrane de la cellule.
Dans différentes parties de la cellule, y compris la partie la plus externe de la membrane cellulaire, des produits chimiques appelés enzymes coupent l'APP en petits morceaux. Ces enzymes qui coupent la PPA sont l'alpha-secrétase, la bêta-secrétase et la gamma-secrétase. Selon l'enzyme qui coupe et les parties de l'APP qui sont coupées, deux choses différentes peuvent se produire. Une qui est utile et une qui provoque la formation de plaques bêta-amyloïdes.
Les plaques sont formées lorsque la bêta-secrétase coupe la molécule APP à une extrémité du peptide bêta-amyloïde, libérant ainsi sAPPβ de la cellule. La gamma-secrétase coupe ensuite les morceaux d'APP restants et, qui dépassent encore de la membrane du neurone, à l'autre extrémité du peptide bêta-amyloïde. Après cette coupure, le peptide bêta-amyloïde est libéré dans l'espace à l'extérieur du neurone et commence à se coller aux autres peptides bêta-amyloïdes. Ces morceaux se collent les uns aux autres pour former des oligomères. Différents oligomères de tailles diverses flottent maintenant dans les espaces entre les neurones, ce qui peut être responsable de la réaction avec les récepteurs des cellules et synapses voisines, affectant leur capacité à fonctionner.
Certains de ces oligomères sont éliminés du cerveau. Ceux qui ne sont pas éliminés se regroupent avec d'autres morceaux de bêta-amyloïde. Plus les morceaux s'agglutinent, plus les oligomères grossissent, et la taille suivante est appelée protofibrilles et la taille suivante est appelée fibrilles. Au bout d'un certain temps, ces fibrilles s'agglutinent avec d'autres molécules de protéines, des neurones et des cellules non nerveuses flottant dans l'espace entre les cellules et forment ce qu'on appelle des plaques.
Angiopathie amyloïde cérébrale (CAA)
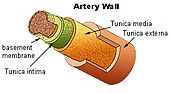
Des dépôts de bêta-amyloïde se forment également dans les parois (dans la tunique moyenne, la couche intermédiaire, et la tunique adventice ou tunique externe, la couche externe) des artères de petite et moyenne taille (et parfois des veines) du cortex cérébral et des leptomeninges (les leptomeninges sont les deux couches internes - pia mater et arachnoïde - des méninges, une membrane protectrice à trois couches recouvrant le cerveau).
La CAA est présente chez 30 % des personnes de plus de 60 ans qui ne souffrent d'aucune démence, mais elle est présente chez 90 à 96 % des personnes atteintes de la maladie d'Alzheimer et est grave dans un tiers à deux tiers de ces cas.


-MRI.png)