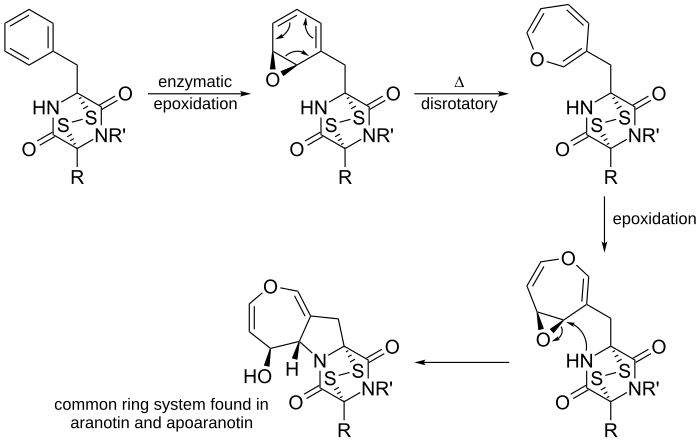
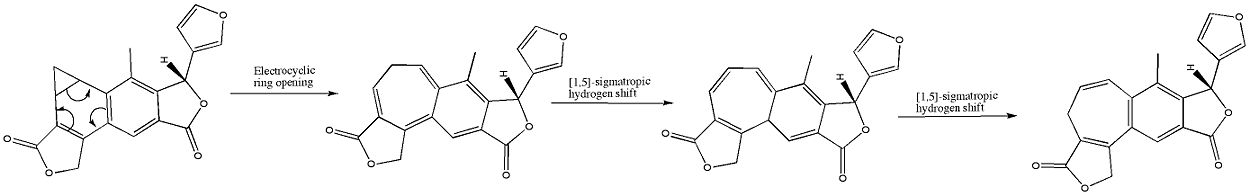
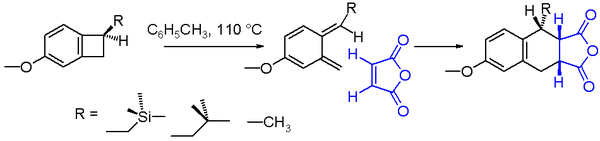
En chimie organique, une réaction électrocyclique est un type de réaction de réarrangement péricyclique. La réaction est électrocyclique si le résultat est qu'une liaison pi devient une liaison sigma ou qu'une liaison sigma devient une liaison pi. Les réactions électrocycliques partagent les propriétés suivantes :
- les réactions électrocycliques sont provoquées par la lumière (photoinduite) ou la chaleur (thermique)
- le mode de réaction est déterminé par le nombre d'électrons pi dans la partie comportant le plus de liaisons pi
- une réaction électrocyclique peut fermer un cycle (électrocyclage) ou ouvrir un cycle
- la stéréospécificité est déterminée par la formation d'un état de transition conrotatoire ou disrotatoire, comme le prévoient les règles de Woodward-Hoffmann.
La torquosélectivité dans une réaction électrocyclique fait référence au sens de rotation des substituants. Par exemple, les substituants dans une réaction qui est conrotative peuvent toujours tourner dans deux directions. Elle produit un mélange de deux produits qui sont l'image miroir l'un de l'autre (produits énantiomériques). Une réaction qui est torquosélective restreint l'un de ces sens de rotation (partiellement ou complètement) pour produire un produit en excès énantiomérique (où un stéréoisomère est produit beaucoup plus que l'autre).
Les chimistes s'intéressent aux réactions électrocycliques car la géométrie des molécules confirme un certain nombre de prédictions faites par les chimistes théoriciens. Ils confirment la conservation de la symétrie orbitale des molécules.
La réaction de cyclisation de Nazarov est une réaction électrocyclique qui ferme un anneau. Elle convertit les divinylcétones en cyclopenténones. (Elle a été découverte par Ivan Nikolaevich Nazarov (1906-1957)).
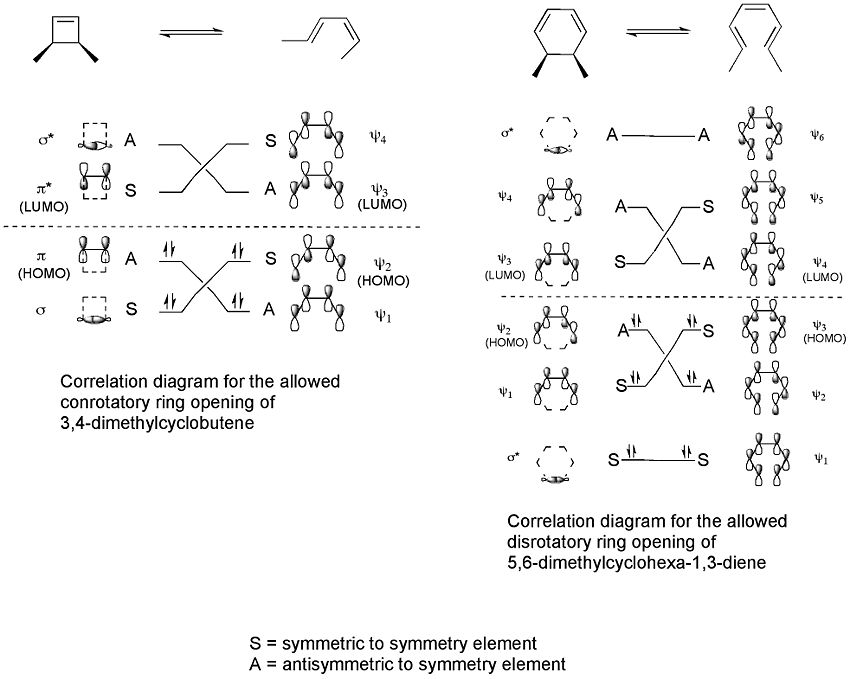
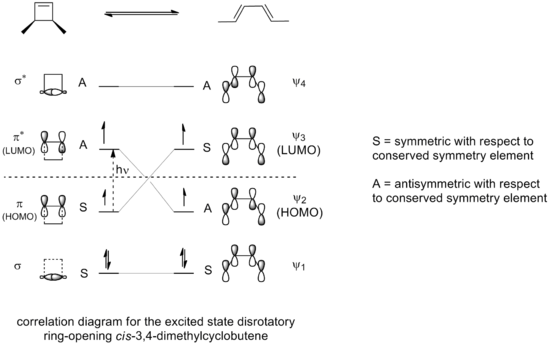
Un exemple est la réaction d'ouverture de cycle thermique du 3,4-diméthylcyclobutène. L'isomère cis ne donne que le cis,trans-2,4-hexadiène. Mais l'isomère trans donne le trans,trans diène :
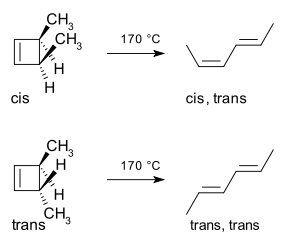
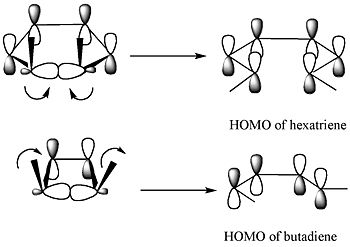
La méthode de la frontière-orbite explique comment cette réaction fonctionne. La liaison sigma dans le réactif s'ouvrira de telle sorte que les p-orbitaux résultants auront la même symétrie que l'orbite moléculaire la plus occupée (HOMO) du produit (un butadiène). Cela ne peut se produire qu'avec une ouverture conrotative de l'anneau qui entraîne des signes opposés pour les deux lobes aux extrémités brisées de l'anneau. (Une ouverture de l'anneau de rotation formerait une anti-liaison.) Le schéma suivant le montre :
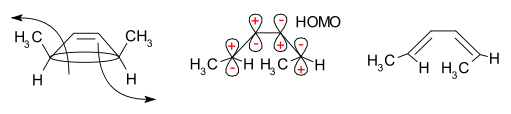
La stéréospécificité du résultat dépend du fait que la réaction passe par un processus conrotatif ou disrotatif.