La chaleur peut faire en sorte que les doubles liaisons forment un anneau. Les cycloadditions thermiques ont généralement (4n + 2) π électrons participant au matériau de départ, pour un nombre entier n. En raison de la symétrie orbitale, la plupart des cycloadditions sont suprafaciales-suprafaciales. Rarement, elles sont antarafaciales-antarafaciales. Il existe quelques exemples de cycloadditions thermiques qui ont 4n électrons π (par exemple la cycloaddition [2 + 2]). Ces cycles se déroulent dans un sens supra-antarafacial. Par exemple, la dimérisation du cétène a un ensemble orthogonal de p orbitales. Ces p orbitales permettent à la réaction de se dérouler en utilisant un état de transition croisée.
La lumière peut également faire en sorte que les doubles liaisons forment un anneau. Des conditions de charge cyclique auxquelles participent 4n π électrons peuvent également se produire à la suite d'une activation photochimique. Ici, un composant fait passer un électron de l'orbite moléculaire la plus haute occupée (HOMO) (π liaison) à l'orbite moléculaire la plus basse inoccupée (LUMO) (π* antiliaison). Une fois que l'électron est promu à l'orbitale supérieure, la symétrie orbitale permet à la réaction de se dérouler de manière supra-faciale et supra-supra-faciale. La réaction de DeMayo en est un exemple. Un autre exemple est montré ci-dessous, la dimérisation photochimique de l'acide cinnamique.
Notez que toutes les cyclisations photochimiques (2+2) ne sont pas des cyclotditions ; certaines sont connues pour fonctionner par des mécanismes radicaux.
Certaines liaisons cycload au lieu de π fonctionnent par le biais d'anneaux de cyclopropane tendus ; car ceux-ci ont un caractère π important. Par exemple, un analogue de la réaction de Diels-Alder est la réaction quadricyclane-DMAD :
Dans la notation (i+j+...) de la cycloaddition, i et j font référence au nombre d'atomes impliqués dans la cycloaddition. Dans cette notation, une réaction de Diels-Alder est une (4+2)cycloaddition et une addition 1,3-dipolaire telle que la première étape de l'ozonolyse est une (3+2)cycloaddition. Cette notation utilise des parenthèses. L'UICPA a toutefois préféré la notation avec [i+j+...] qui compte les électrons et non les atomes. Elle utilise des crochets. Dans cette notation, la réaction de Diels-Alder et la réaction dipolaire deviennent toutes deux une [4+2]cycloaddition. La réaction entre le norbornadiène et un alcyne activé est une [2+2+2]cycloaddition.
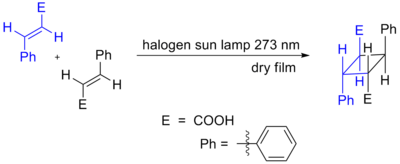
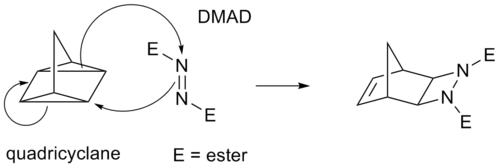
.png)
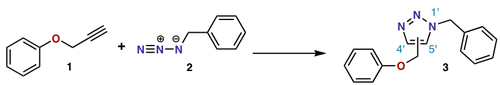
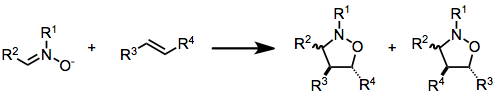
![Intermolecular Formal [3+3] Cycloaddition Reaction](https://www.alegsaonline.com/image/600px-3+3-cycloaddition.svg.png)