Les liaisons covalentes sont des liaisons chimiques entre deux atomes non métalliques. Un exemple est l'eau, où l'hydrogène (H) et l'oxygène (O) se lient ensemble pour former (H2O). Une enveloppe extérieure pleine comporte généralement huit électrons, ou deux dans le cas de l'hydrogène ou de l'hélium. Les électrons de valence sont les électrons maintenus de manière relativement lâche dans l'enveloppe extérieure de l'atome. La structure des coquilles d'électrons est déterminée par la mécanique quantique).
Le nombre d'électrons dans un atome est décidé par le nombre de protons dans l'atome. Les électrons sont en orbite autour des noyaux atomiques, et ils sont comme des trajectoires orbitales floues autour d'un noyau atomique. La première couche contient jusqu'à deux électrons. Les couches suivantes contiennent généralement jusqu'à huit électrons. Les liaisons covalentes sont formées par des atomes partageant des électrons de valence.
Si, par exemple, un atome a neuf électrons, les deux premiers orbitent très près du noyau, les sept suivants orbitent un peu plus loin. Les sept électrons extérieurs sont moins serrés que les deux électrons intérieurs car ils sont plus éloignés du noyau chargé positivement. Si cet atome se rapproche d'un autre atome, avec un électron mal tenu dans son enveloppe extérieure, une nouvelle orbite sera disponible pour l'électron mal tenu. Cette nouvelle orbite électronique est liée aux deux noyaux atomiques et a un niveau d'énergie inférieur à celui de l'orbite électronique d'origine. L'électron peut spontanément sauter vers elle et émettre un photon avec l'énergie excédentaire. Nous avons maintenant un électron en orbite autour des deux atomes, ce qui fait que l'atome qui a fourni l'électron a une petite charge positive nette et l'autre atome a une petite charge négative nette. Les deux atomes sont maintenant maintenus ensemble par la force d'attraction électromagnétique entre les charges positives et négatives. C'est ce que l'on appelle une liaison covalente. Pour rompre cette liaison, il faut la même quantité d'énergie que celle qui a été libérée lors de sa formation.
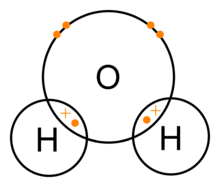
Une molécule d'eau est constituée d'un atome d'oxygène et de deux atomes d'hydrogène maintenus ensemble par une liaison covalente. Dans ce cas, l'atome d'oxygène partage un électron avec chaque atome d'hydrogène. Cela signifie que les atomes d'oxygène ont une petite charge positive nette et l'atome d'hydrogène une petite charge négative nette. Par conséquent, les atomes d'oxygène et d'hydrogène sont attirés l'un vers l'autre par la force électromagnétique. C'est pourquoi la molécule d'eau est une molécule polaire : sa charge n'est pas uniformément répartie.