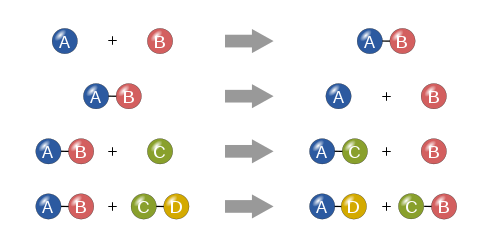
Synthèse
Dans une réaction de synthèse, deux ou plusieurs substances simples se combinent pour former une substance plus complexe.
A + B ⟶ A B {\displaystyle A+B\longrightarrow AB}
"Deux ou plusieurs réactifs donnant un produit" est une autre façon d'identifier une réaction de synthèse. Un exemple de réaction de synthèse est la combinaison du fer et du soufre pour former du sulfure de fer(II) :
8 F e + S 8 ⟶ 8 F e S {\displaystyle 8Fe+S_{8}\longrightarrow 8FeS}
Un autre exemple est celui de l'hydrogène gazeux simple combiné à de l'oxygène gazeux simple pour produire une substance plus complexe, comme l'eau.
Décomposition
Une réaction de décomposition se produit lorsqu'une substance plus complexe se décompose en ses parties plus simples. Elle est donc l'opposé d'une réaction de synthèse, et peut s'écrire comme :
A B ⟶ A + B {\displaystyle AB\longrightarrow A+B}
Un exemple de réaction de décomposition est l'électrolyse de l'eau pour produire de l'oxygène et de l'hydrogène gazeux :
2 H 2 O ⟶ 2 H 2 + O 2 {\displaystyle 2H_{2}O\longrightarrow 2H_{2}+O_{2}}
Remplacement unique
Dans une réaction de remplacement unique, un élément non combiné en remplace un autre dans un composé ; en d'autres termes, un élément échange des places avec un autre élément dans un composé Ces réactions se présentent sous la forme générale de
A + B C ⟶ A C + B {\displaystyle A+BC\longrightarrow AC+B}
Un exemple de réaction de déplacement unique est lorsque le magnésium remplace l'hydrogène dans l'eau pour produire de l'hydroxyde de magnésium et de l'hydrogène gazeux :
M g + 2 H 2 O ⟶ M g ( O H ) 2 + H 2 {\displaystyle Mg+2H_{2}O\longrightarrow Mg(OH)_{2}+H_{2}}
Double remplacement
Dans une double réaction de remplacement, les anions et les cations de deux composés changent de place et forment deux composés entièrement différents. Ces réactions se présentent sous la forme générale :
A B + C D ⟶ A D + C B {\displaystyle AB+CD\longrightarrow AD+CB}
Par exemple, lorsque le chlorure de baryum (BaCl2) et le sulfate de magnésium (MgSO4) réagissent, l'anion SO42- change de place avec l'anion 2Cl-, donnant les composés BaSO4 et MgCl2.
Un autre exemple de réaction à double déplacement est la réaction du nitrate de plomb(II) avec l'iodure de potassium pour former de l'iodure de plomb(II) et du nitrate de potassium :
P b ( N O 3 ) 2 + 2 K I ⟶ P b I 2 + 2 K N O 3 {\displaystyle Pb(NO_{3})_{2}+2KI\longrightarrow PbI_{2}+2KNO_{3}}