Cinétique chimique
La cinétique chimique, également appelée cinétique des réactions, étudie la vitesse à laquelle se déroulent les réactions chimiques. Cela inclut l'étude de la manière dont différentes conditions telles que la température, la pression ou le solvant utilisé affectent la vitesse d'une réaction. La cinétique chimique peut également être utilisée pour découvrir les mécanismes de réaction et les états de transition.
L'idée de base de la cinétique chimique est appelée théorie des collisions. Celle-ci stipule que pour qu'une réaction ait lieu, les molécules doivent se heurter les unes aux autres. Les moyens d'augmenter la vitesse de la réaction doivent donc augmenter le nombre de collisions. Cela peut se faire de plusieurs façons.
Grâce à des expériences, il est possible de calculer des taux de réaction à partir desquels vous pouvez obtenir des lois et des constantes de taux. Une loi de vitesse est une expression mathématique avec laquelle vous pouvez calculer la vitesse d'une réaction en fonction de la concentration des réactifs.
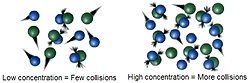
Avec une concentration plus élevée, les molécules s'entrechoquent plus facilement et la vitesse de réaction est donc plus grande
Ordre d'une réaction
l'équilibre est de nature dynamique
Il existe de nombreux types de lois sur les tarifs, mais les plus courantes sont les suivantes :
- réaction d'ordre zéro : la vitesse ne dépend pas de la concentration
- réaction de premier ordre : la vitesse dépend de la concentration d'un seul réactif
- réaction de second ordre : la vitesse dépend de la concentration de deux réactifs, ou de la concentration d'un réactif au carré.
A partir de ces données, il est possible de réfléchir au mécanisme de la réaction. S'il est de second ordre, par exemple, il est probable que les deux molécules de la réaction se rejoignent lors de l'étape de détermination de la vitesse. C'est l'étape la plus difficile du mécanisme à franchir, car elle présente la plus grande énergie d'activation.
| · v · t · e Mécanismes de réaction de base | |
| Substitution nucléophile | Substitution nucléophile unimoléculaire (SN1) - Substitution nucléophile bimoléculaire (SN2) - Substitution nucléophile aromatique (SNAr) - Substitution nucléophile interne (SNi) |
| Réaction d'élimination | Élimination unimoléculaire (E1) - Réaction d'élimination E1cB - Élimination bimoléculaire (E2) |
| Réactions d'addition | Addition électrophile - Addition nucléophile - Addition de radicaux libres - Cycloaddition |
| Sujets connexes | Réaction élémentaire - Molécularité - Stéréochimie - Catalyse - Théorie des collisions - Effets des solvants - Poussée des flèches |
| Cinétique chimique | Équation de taux - Échelon de détermination du taux |
Questions et réponses
Q : Qu'est-ce que la cinétique chimique ?
R : La cinétique chimique, également appelée cinétique des réactions, est l'étude de la vitesse des réactions chimiques et de la façon dont différentes conditions telles que la température, la pression ou le solvant utilisé affectent la vitesse d'une réaction.
Q : Que dit la théorie des collisions ?
R : La théorie des collisions stipule que pour qu'une réaction se produise, les molécules doivent se heurter les unes aux autres. Les moyens d'augmenter la vitesse de la réaction doivent donc augmenter le nombre de collisions.
Q : Comment pouvez-vous calculer les taux de réaction ?
R : Grâce à des expériences, il est possible de calculer les vitesses de réaction à partir desquelles vous pouvez obtenir des lois et des constantes de vitesse.
Q : Qu'est-ce qu'une loi de vitesse ?
R : Une loi de vitesse est une expression mathématique permettant de calculer la vitesse d'une réaction en fonction de la concentration des réactifs.
Q : Comment pouvez-vous augmenter la vitesse d'une réaction ?
R : La vitesse d'une réaction peut être augmentée en augmentant le nombre de collisions entre les molécules. Cela peut se faire de plusieurs façons, par exemple en modifiant la température, la pression ou le solvant utilisé.
Q : Que sont les états de transition ?
R : Les états de transition sont des étapes intermédiaires des réactions chimiques qui se produisent lorsque les réactifs forment des produits et que de l'énergie est libérée ou absorbée au cours de ce processus.
Rechercher dans l'encyclopédie