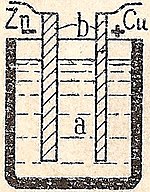
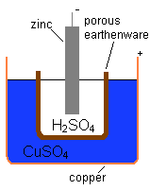
Une cellule électrochimique qui provoque un flux de courant électrique externe peut être créée en utilisant deux métaux différents, car les métaux ont une tendance différente à perdre des électrons. Le zinc perd plus facilement des électrons que le cuivre. Ainsi, en plaçant le zinc et le cuivre métallique dans des solutions de leurs sels, on peut faire circuler des électrons à travers un fil externe qui mène du zinc au cuivre. Lorsqu'un atome de zinc fournit les électrons, il devient un ion positif et passe en solution aqueuse, ce qui diminue la masse de l'électrode de zinc. Du côté du cuivre, les deux électrons reçus lui permettent de convertir un ion cuivre de la solution en un atome de cuivre non chargé qui se dépose sur l'électrode de cuivre, augmentant ainsi sa masse. Les deux réactions s'écrivent généralement
Zn(s) --> Zn2+(aq) + 2e-
Cu2+(aq) + 2e- --> Cu(s)
Les lettres entre parenthèses rappellent que le zinc passe d'un solide (s) à une solution aqueuse (aq) et inversement pour le cuivre. Il est typique dans le langage de l'électrochimie de désigner ces deux processus comme des "demi-réactions" qui se produisent aux deux électrodes.
| Zn(s) -> Zn2+(aq) + 2e- | | La "demi-réaction" du zinc est classée comme une oxydation car elle perd des électrons. La borne à laquelle l'oxydation se produit est appelée "anode". Pour une batterie, c'est la borne négative. | |
| La "demi-réaction" du cuivre est classée comme une réduction puisqu'elle gagne des électrons. La borne à laquelle la réduction se produit est appelée "cathode". Pour une batterie, c'est la borne positive. | | Cu2+(aq) + 2e- -> Cu(s) |
Pour que la cellule voltaïque continue à produire un courant électrique externe, il faut que les ions sulfate en solution se déplacent de droite à gauche pour équilibrer le flux d'électrons dans le circuit externe. Les ions métalliques eux-mêmes doivent être empêchés de se déplacer entre les électrodes, de sorte qu'une sorte de membrane poreuse ou un autre mécanisme doit permettre le mouvement sélectif des ions négatifs dans l'électrolyte de la droite vers la gauche.
De l'énergie est nécessaire pour forcer les électrons à passer de l'électrode de zinc à l'électrode de cuivre, et la quantité d'énergie par unité de charge disponible de la cellule voltaïque est appelée force électromotrice (emf) de la cellule. L'énergie par unité de charge est exprimée en volts (1 volt = 1 joule/coulomb).
Il est clair que pour obtenir de l'énergie de la cellule, il faut que l'oxydation du zinc libère plus d'énergie qu'il n'en faut pour réduire le cuivre. La cellule peut produire une quantité limitée d'énergie à partir de ce processus, le processus étant limité par la quantité de matériau disponible soit dans l'électrolyte, soit dans les électrodes métalliques. Par exemple, s'il y avait une mole d'ions sulfate SO42- du côté du cuivre, le processus se limiterait à transférer deux moles d'électrons par le circuit externe. La quantité de charge électrique contenue dans une mole d'électrons est appelée constante de Faraday, et est égale au nombre de fois la charge de l'électron selon Avogadro :
Constante de Faraday = F = NAe = 6,022 x 1023 x 1,602 x 10-19 = 96 485 Coulombs/mole
Le rendement énergétique d'une cellule voltaïque est donné par la tension de la cellule multipliée par le nombre de moles d'électrons transférés multiplié par la constante de Faraday.
Production d'énergie électrique = nFEcell
La force électromotrice de la cellule peut être prédite à partir des potentiels d'électrode standard des deux métaux. Pour la cellule zinc/cuivre dans les conditions standard, le potentiel de cellule calculé est de 1,1 volt.