Thermodynamique
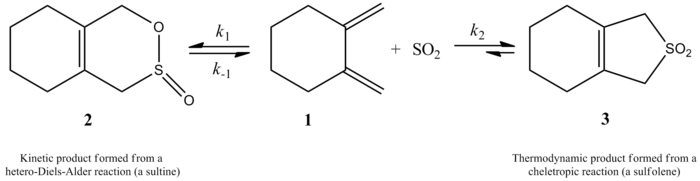
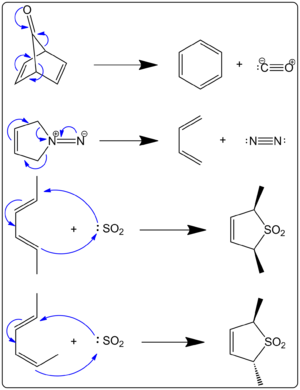
Lorsque le dioxyde de soufre réagit avec le butadiène et l'isoprène, il en résulte deux produits différents. Le mécanisme de réaction contrôlera ce qui sera fabriqué. Un produit cinétique et un produit thermodynamique sont tous deux possibles. Le produit thermodynamique est plus important que le produit cinétique. Le produit cinétique provient d'une réaction de Diels-Alder, tandis qu'une réaction chélétropique donne un produit thermodynamiquement plus stable. La voie chélétropique est davantage utilisée car elle donne un produit d'addition cyclique à cinq membres plus stable. Le schéma ci-dessous montre la différence entre les deux produits. Le chemin vers la gauche montre le produit thermodynamique, tandis que le chemin vers la droite montre le produit cinétique. Suarez et Sordo l'ont montré en 1995. Ils l'ont montré à la fois par des expériences et en utilisant des calculs gaussiens.
Cinétique
Un exemple en est les réactions chélétropes des 1,3-diènes avec le dioxyde de soufre. Les chimistes ont étudié avec soin la cinétique de cette réaction. En 1976, Isaacs et Laila ont mesuré les facteurs cinétiques de l'addition de dioxyde de soufre aux dérivés du butadiène. Les taux d'addition ont été contrôlés dans du benzène à 30 °C avec un excès initial de diène vingt fois supérieur. Ils ont utilisé un spectrophotomètre pour étudier la lumière à 320 nm afin de mesurer la disparition du SO2. La réaction a montré une "pseudo-cinétique du premier ordre". Les chimistes ont découvert que les groupes attracteurs d'électrons sur le diène diminuaient la vitesse de réaction. De plus, la vitesse de réaction a été considérablement affectée par les effets stériques des substituts 2, des groupes plus volumineux augmentant la vitesse de réaction. (En d'autres termes, plus le groupe d'atomes accrochés au second atome de carbone est grand, plus la réaction est rapide). Les auteurs attribuent cela à la tendance des groupes volumineux à favoriser la conformation cisoïde du diène qui est essentielle à la réaction (voir tableau ci-dessous). En outre, les taux à quatre températures ont été mesurés pour sept des diènes. À partir de ces mesures, les chimistes ont utilisé l'équation d'Arrhenius pour calculer l'enthalpie d'activation (ΔH‡) et l'entropie d'activation (ΔS‡) pour chaque réaction. Ce fut l'un des premiers efforts importants pour étudier la génétique d'une réaction chélétropique.
| -Butadiène | 104 k /min-1 (30 °C) (± 1-2%) absolu | 104 k /min-1 (30 °C) (± 1-2%) relatif | ΔH‡ /kcal mol-1 | ΔS‡ /cal mol-1 K-1 |
| 2-méthyle | 1.83 | 1.00 | 14.9 | -15 |
| 2-éthyle | 4.76 | 2.60 | 10.6 | -20 |
| 2-isopropyle | 13.0 | 7.38 | 12.5 | -17 |
| 2-tert-butyl | 38.2 | 20.8 | 10.0 | -19 |
| 2-neopentyl | 17.2 | 9.4 | 11.6 | -18 |
| 2-cloro | 0.24 | 0.13 | N/A | N/A |
| 2-bromoéthyle | 0.72 | 0.39 | N/A | N/A |
| 2-p-tolyl | 24.7 | 13.5 | 10.4 | -19 |
| 2-phényle | 17.3 | 9.45 | N/A | N/A |
| 2-(p-bromophényle) | 9.07 | 4.96 | N/A | N/A |
| 2,3-diméthyle | 3.54 | 1.93 | 12.3 | -18 |
| cis-1-méthyle | 0.18 | 0.10 | N/A | N/A |
| trans-1-méthyle | 0.69 | 0.38 | N/A | N/A |
| 1,2-diméthylène-cyclohexane | 24.7 | 13.5 | 11.4 | -16 |
| 2-méthyl-1,1,4,4-d4 | 1.96 | N/A | N/A | N/A |
En 2002, Monnat, Vogel et Sordo ont mesuré la cinétique d'addition du dioxyde de soufre aux 1,2-diméthylidènecycloalcanes. Ils ont écrit que la réaction du 1,2-diméthylidènecyclohexane avec le dioxyde de soufre peut donner deux produits différents en fonction des conditions de réaction. La réaction donne la sultine correspondante par une réaction d'hétéro-Diels-Alder sous contrôle cinétique (≤ -60 °C), mais, sous contrôle thermodynamique (≥ -40 °C), la réaction donne le sulfolène correspondant par une réaction chélétropique. L'enthalpie d'activation de la réaction hétéro-Diels-Alder est inférieure d'environ 2 kcal/mol à celle de la réaction chélétrophique correspondante. Le sulfolène est environ 10 kcal/mol plus stable que la sultine isométrique en solution de CH2Cl2/SO2.
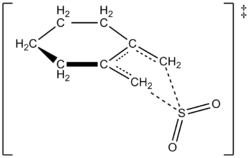
Les auteurs ont pu élaborer expérimentalement une loi de taux à 261,2 K pour la réaction du 1,2-diméthylidènecyclohexane avec le dioxyde de soufre afin de donner le sulfolène correspondant. La réaction était du premier ordre pour le 1,2-diméthylidènecyclohexane, mais du second ordre pour le dioxyde de soufre (voir ci-dessous). Cela a confirmé une prédiction des chimistes théoriciens basée sur des calculs quantiques ab initio de haut niveau. À l'aide de méthodes de calcul, les auteurs ont proposé une structure de transition pour la réaction chélétropique du 1,2-diméthylidènecyclohexane avec le dioxyde de soufre (voir la figure de droite). La réaction est du second ordre pour le dioxyde de soufre car une autre molécule de dioxyde de soufre se lie probablement à l'état de transition pour aider à le stabiliser. Des résultats similaires ont été trouvés dans une étude réalisée en 1995 par Suarez, Sordo et Sordo qui a utilisé des calculs ab initio pour étudier le contrôle cinétique et thermodynamique de la réaction du dioxyde de soufre avec les 1,3-diènes.
d [ 3 ] d t = k 2 [ 1 ] [ S O 2 ] 2 {\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)
Effets des solvants
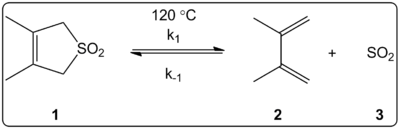
L'effet du solvant de la réaction chélétropique du 3,4-diméthyl-2,5-dihydrothiophène-1,1-dioxyde (illustré à droite) a été étudié cinématiquement dans 14 solvants. Les constantes de vitesse de réaction de la réaction directe et de la réaction inverse, en plus des constantes d'équilibre, se sont avérées en corrélation linéaire avec l'échelle de polarité des solvants ET(30).
Les réactions ont été effectuées à 120 °C et ont été étudiées par spectroscopie RMN 1H du mélange réactionnel. On a constaté que la vitesse de propagation k1 diminuait d'un facteur de 4,5 en passant du cyclohexane au méthanol. La vitesse inverse k-1 a augmenté d'un facteur de 53 en passant du cyclohexane au méthanol, tandis que la constante d'équilibre Keq a diminué d'un facteur de 140. Il est suggéré qu'il y a un changement de la polarité pendant le processus d'activation comme le montrent les relations entre l'équilibre et les données cinétiques. Les auteurs affirment que la réaction semble être influencée par la polarité du solvant, ce qui peut être démontré par le changement des moments dipolaires lors du passage du réactif à l'état de transition vers le produit. Les auteurs affirment également que la réaction chélétrophique ne semble pas être influencée par l'acidité ou la basicité du solvant.
Les résultats de cette étude conduisent les auteurs à s'attendre aux comportements suivants :
1. Le changement de la polarité du solvant influence moins le taux que l'équilibre.
2. Les constantes de vitesse seront caractérisées par un effet inverse sur la polarité : k1 diminuera légèrement avec l'augmentation de ET(30), et k-1 augmentera dans les mêmes conditions.
3. L'effet sur le k-1 sera plus important que sur le k1.

![{\displaystyle {\frac {d[3]}{dt}}=k_{2}[1][SO_{2}]^{2}}](https://www.alegsaonline.com/image/a02f69dd0783356fbf24499f57d0df29cd264f16.svg)