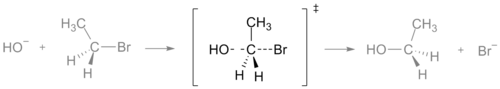Dans une réaction chimique, l'état de transition est le point où il y a une valeur maximale d'énergie. Cette énergie est appelée l'énergie d'activation. Lorsque deux ou plusieurs molécules sont mélangées, elles se heurtent les unes aux autres. Si elles se heurtent avec suffisamment d'énergie pour passer par l'état de transition, elles réagiront et formeront de nouvelles molécules. À l'état de transition, de nouvelles liaisons sont formées tandis que les anciennes sont rompues. Dans un graphique ou un dessin, l'état de transition est souvent marqué par le symbole de la double dague ‡.
Il est très difficile d'étudier un état de transition. En effet, il est si riche en énergie que les molécules restent sous cette forme pendant un temps très court, généralement des femtosecondes. Il est important de ne pas confondre les états de transition avec les intermédiaires. Les intermédiaires se trouvent à des points d'énergie minimale et peuvent vivre très longtemps. Comme un état de transition, cependant, un intermédiaire se trouve entre les réactifs et les produits d'une réaction.
L'étude des états de transition est très importante pour comprendre les mécanismes de réaction. Il existe des théories et des programmes informatiques qui peuvent être utilisés pour calculer à quoi ressemble l'état de transition. C'est une partie de la cinétique chimique.